Загальні відомості про периферичну нейропатію і нейропатичний біль
Периферична нейропатія (ПН) є досить поширеним станом, за оцінками, захворюваність на неї у світі становить 2,4 % у загальній популяції, при цьому може досягати 8 % в осіб похилого віку і 50 % — у діабетиків.
Нейропатія має різні причини, що включать здавлювання нервів (корінцеві й периферичні), цукровий діабет, авітаміноз, вірусну інфекцію (особливо ура-ження герпесвірусом), васкуліти й імунні захворювання, багато з яких є ідіопатичними. Пацієнти з ПН часто скаржаться на пекучий, колючий біль або відчуття електричного удару — так званий нейропатичний біль, також нерідко зустрічаються алодинія і гіпералгезія.
Міжнародна асоціація з вивчення болю (IASP) визначає нейропатичний біль як біль, що виникає у зв’язку з пошкодженням або захворюванням соматосенсорної (периферичної і/або центральної) нервової системи. Нейропатичний біль зазвичай має хронічний перебіг (~3 місяці), проявляється постійно або періодично рецидивує.
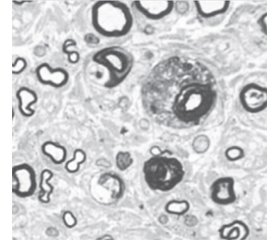
Нейропатії, що лежать в основі периферичного нейропатичного синдрому, патоморфологічно характе-ризуються такими порушеннями: валерова дегенерація, дистальна аксонопатія, сегментарна демієлінізація і їх поєднання.
Валерова дегенерація виникає тоді, коли цілісність нерва порушена. Дистальний (нижче від місця травми) аксон і його мієлінова оболонка резорбуються. А з проксимального (вище від місця травми) фрагмента нерва відростає новий аксон і покривається мієліновою оболонкою. Валерова дегенерація зустрічається, наприклад, при травматичних нейропатіях.
При дистальній аксонопатії дегенерація аксона й мієліну починається в найвіддаленіших ділянках нерва, а потім піднімається звідти вгору по ходу нерва. Дистальна аксонопатія характерна, наприклад, для діабетичної полінейропатії.
При сегментарній демієлінізації аксон залишається цілим, а мієлін руйнується на окремих фрагментах нерва. Сегментарна демієлінізація зустрічається, наприклад, при люмбосакральній радикулопатії.
Зниження якості життя, зміна настрою і порушення сну є загальними явищами й основними причинами професійної інвалідності. Патофізіологія ПН часто передбачає ураження клітин Шванна, що продукують мієлін, у периферичних нервах. Це ураження може відрізнятися за ступенем тяжкості й виглядом. Регенерація і підтримка мієлінової оболонки після ураження нерва є важливим елементом лікування ПН. Ураження периферичних нервів призводять до втрати рухової, сенсорної і вегетативної функції в дистальних денервованих сегментах унаслідок порушення аксона, дегенерації нервових волокон і навіть загибелі нейронів.
Механізми дії
Уридинмонофосфат, вітамін В12 (ціанокобаламін) і фолієва кислота — ці середники беруть участь у метаболічних процесах і таким чином сприяють регенерації нервових волокон і чинять непряму (вторинну) знеболювальну дію. Крім того, похідні уридинмонофосфату стимулюють пуринергічні P2Y-рецептори, проявляючи пряму (первинну) знеболювальну й стимулюючу регенераційну дію. Потрапляючи в організм, ціанокобаламін перетворюється на кобаламін, а потім на метилкобаламін і аденозилкобаламін (активні форми вітаміну В12); фолієва кислота перетворюється на 5-метилтетрагідрофолат, 5,10-метилентетрагідрофолат і 10-формілтетрагідрофолат (активні форми фолієвої кислоти). Фолієва кислота, всмоктуючись у кишечнику, перетворюється на 5-метілтетрагідрофолат, який шляхом низки змін перетворюється на метіонін. Метіонін необхідний для синтезу білків, РНК, ДНК, фосфатидилхоліну, мієліну, нейромедіаторів тощо. 5,10-метилентетрагідрофолат і 10-формілтетрагідрофолат беруть участь в утворенні піримідинових і пуринових нуклеотидів, необхідних для побудови РНК і ДНК.
Лікування пацієнтів з невропатичним болем (НБ) у разі множинних супутніх захворювань — складний мультидисциплінарний процес, що вимагає медикаментозної терапії, психологічної реабілітації і фізіотерапевтичного впливу. Незважаючи на доведену низьку ефективність нестероїдних протизапальних препаратів (НПЗП) і анальгетиків у цих хворих, близько 2/3 з них отримують зазначені препарати. Неправильний вибір тактики лікування у хворих із НБ спричиняє зниження його ефективності й істотне збільшення тривалості лікування й витрат. При цьому лише незначна частка лікарів використовує у своїй клінічній практиці повний перелік рекомендованих лікарських засобів, які можна було б застосувати як препарати першої лінії для купірування НБ.
/38.jpg)
Ефективність застосування нуклеотидів при терапії пацієнтів із НБ доведена в низці досліджень. Так, у ретроспективному дослідженні (Lauretti G.R. et al., 2004) оцінювали ефект застосування комбінації цитидину, уридину з вітаміном B12 в якості допоміжної терапії при лікуванні хронічного нейропатичного поперекового болю в пацієнтів з каудальним введенням клонідину, лідокаїну й дексаметазону. Усього в дослідженні взяли участь 42 пацієнти: 21 — направлений на проведення каудальної блокади (контрольна група), 21 — отримував комбінацію «цитидин + уридин + вітамін B12» 2 рази на добу протягом 28 днів. Результати продемонстрували, що в контрольній групі була вищою потреба в застосуванні пероральних НПЗП, ніж у групі прийому комбінації «цитидин + уридин + вітамін B12», що свідчить про ефективність застосування комбінації нуклеотидів з вітаміном В12 у терапії НБ у спині. У нещодавніх дослідженнях оцінювали ефективність і безпеку застосування комбінації «уридин-5’-динатрію монофосфат + фолієва кислота + вітамін В12» у 212 пацієнтів із НБ. Результати продемонстрували статистично значуще зменшення загальної оцінки болю за опитувальником болю (pain DETECT Questionnaire — PDQ), інтенсивності больового синдрому, кількості уражених ділянок і ступеня больового відчуття в пацієнтів, які приймали комбінацію нуклеотидів (Negrão L. et al., 2014; Negrão L., Nunes P., 2015). На сьогодні є небагато препаратів, які би діяли на рівні периферичних нервів і сприяли б їх фізіологічній регенерації. Тому застосування комплексу Нейрістон, до складу якого входить уридин-5’-динатрію монофосфат, вітамін В12 і фолієва кислота, що дають регенераторний і знеболювальний ефекти, у комбінованій терапії може покращити ефективність лікування НБ. Активні компоненти комплексу Нейрістон сприяють активізації власних відновних процесів у пошкоджених нервових тканинах. Уридинмонофосфат, який є основним його компонентом, стимулює синтез фосфоліпідів, гліколіпідів (сфінголіпідів) і глікопротеїнів — основних структурних компонентів клітинних мембран, що забезпечує його регенеративний вплив на нервові волокна. Фолієва кислота й вітамін В12 є необхідними коферментами для більшості метаболічних реакцій, за рахунок чого відіграють важливу роль у синтезі нуклеїнових кислот і білків. Комбінація активних речовин забезпечує комплексний вплив на фізіологічні функції організму й приводить до прискорення відновних процесів у пошкоджених нервових волокнах. Комплекс Нейрістон може бути рекомендований як джерело поживних речовин, що сприяють відновленню пошкоджених нервових волокон при таких станах, як нейропатія, невралгія, люмбаго, ураження нервових структур метаболічного характеру, інфекційні нейропатії тощо.
Периферичний нейропатичний біль після нуклеотомії
Нуклеотомія зводиться до видалення або руйнування пульпозного ядра при лікуванні міжхребцевих гриж. У проспективне контрольоване дослідження були включені 123 пацієнти з болем і функціональними порушеннями після нуклеотомії. З них 83 пацієнти (середній вік 47 років) на додаток до звичайної терапії отримували фіксовану комбінацію уридинмонофосфату 50 мг, ціанокобаламіну 3 мкг і фолієвої кислоти 400 мкг по 1 капсулі на день протягом 3 тижнів. Решта 40 пацієнтів (середній вік 48 років) у ці ж строки отримували звичайну терапію, без додавання фіксованої комбінації (контрольна група). Оцінку загального бала болю проводили за візуальною аналоговою шкалою (можливий діапазон значень від 0 до 100 мм).
У результаті дослідження було з’ясовано, що вираженість болю за візуальною аналоговою шкалою в групі з фіксованою комбінацією мала таку динаміку: спочатку — 90 мм, через 2 тижні — 24 мм, через 3 тижні — 8 мм. У ці ж строки в контрольній групі динаміка болю становила 81, 45 і 30 мм відповідно. Відмінності були вірогідними на користь групи з комбінованою терапією (p < 0,005 для 2 тижнів і p < 0,001 для 3 тижнів). Абсолютне зниження болю становило 91 % у групі з фіксованою комбінацією і 63 % — у контрольній групі. Якість життя за опитувальником QLQ-C30 (відсоток приросту): до 3-го тижня лікування якість життя підвищилася на 64 % у групі з фіксованою комбінацією і на 36 % — у контрольній групі (p < 0,001). Що стосується загального клінічного враження щодо успіху терапії в лікарів і пацієнтів, то, на думку лікарів, на 3-му тижні лікування спостерігалося значне покращання стану у 89 % пацієнтів.
Висновки
У виконаних дослідженнях була продемонстрована клінічна ефективність комбінації уридинмонофосфату 50 мг, ціанокобаламіну 3 мкг і фолієвої кислоти 400 мкг при основних видах периферичного нейропатичного болю (люмбальна/люмбосакральна радикулопатія, цервікальна радикулопатія, карпальний тунельний синдром, діабетична нейропатія тощо). При цьому комбінація не викликала побічних ефектів і добре переносилася.
При лікуванні пацієнтів з нейропатичним болем важливим є комплексний підхід, який включає симптоматичну й патогенетичну терапію. Наявні на сьогодні дані свідчать, що застосування комплексу уридинмонофосфату з ціанокобаламіном і фолієвою кислотою (Нейрістон) сприяє ефективному купіруванню больового синдрому, активізації власних відновних процесів у пошкоджених нервових клітинах, а також покращанню якості життя пацієнтів з нейропатичним больовим синдромом.
Конфлікт інтересів. Не заявлений.
Список литературы
1. Аattal N., Cruccu G., Baron R. et al. European Federation of Neurological Societies: EFNS guidelines on the pharmacological treatment of neuropathic pain: 2010 revision. Eur. J. Neurol. 2010. 17. e1113-e1188.
2. Scholz J., Finnerup N.B., Attal N. et al. The IASP classification of chronic pain for ICD-11: chronic neuropathic pain. Pain. 2019. Vol. 160. № 1. P. 53-59.
3. Szok D., Tajti J., Nyári A., Vécsei L. Therapeutic Approaches for Peripheral and Central Neuropathic Pain. Behav. Neurol. 2019. Vol. 2019. Article ID 8685954.
4. Negrão L., Almeida P., Alcino S. et al. Effect of the combination of uridine nucleotides, folic acid and vitamin B12 on the clinical expression of peripheral neuropathies. Pain Manag. 2014. Vol. 4. № 3. P. 191-196.
5. Finnerup N.B., Attal N. Pharmacotherapy of neuropathic pain: time to rewrite the rulebook. Pain Manag. 2016. 6(1). 1–3.
6. Finnerup N.B., Otto M., McQuay H.J. et al. Algorithm for neuropathic pain treatment — an evidence based proposal. Pain. 2005. 118(3). 289-305.
7. Lauretti G.C., Оmals M., Pereira A.C. et al. Clinical evaluation of the analgesic effect of the cytidine-uridine-hydroxocobalamin complex as a coadjuvant in the treatment of chronic neuropathic low back pain. Column. 2004. 3(2). 73-76.
8. Мartinez V., Аttal N., Bouhassira D. et al. Chronic neuropathic pain: diagnosis, evaluation and treatment in outpatient services. Guidelines for clinical practice of the French Society for the Study and Treatment of Pain. Douleur analg. 2010. 23. 51-66.
9. Мüller D. Treatment of neuropathic pain syndromes. Results of an open study of the efficacy of a preparation based on pyrimidine nucleotides. Munich: Medien und Medizin Verlagsgesellschaft mbH&Co, 2002.
10. Okada M., Nakagawa T., Minami M., Satoh M. Analgesic effects of intrathecal administration of P2Y nucleotide receptor agonists UTP and UDP in normal and neuropathic pain model rats. J. Pharmacol. Exp. Ther. 2002. Vol. 303. № 1. P. 66-73.
11. Negrão L., Аlmeida P., Alcino S. et al. Effect of the combination of uridine nucleotides, folic acid and vitamin B12 on the clinical expression of peripheral neuropathies. Pain Manag. 2014. 4(3). 191-196. doi: 10.2217/pmt.14.10.
12. Suezawa Y., Jacob H.A. Percutaneous nucleotomy. An alternative to spinal surgery. Arch. Orthop. Trauma Surg. 1986. Vol. 105. № 5. P. 287-295.
13. Sheki A.A., Hamdan F.B. The role of different neurophysiological tests in the differential diagnosis of diabetic axonal neuropathy and lumbosacral radiculopathy. Neurosciences (Riyadh). 2009. Vol. 14. № 1. P. 25-30.
14. Manole E., Bastian A., Neagu M. et al. Schwann Cell Plasticity in Peripheral Nerve Regeneration after Injury. 2020. https://www.intechopen.com.
15. Yonezawa T., Onomura T., Kosaka R. et al. The system and procedures of percutaneous intradiscal laser nucleotomy. Spine (Phila. Pa 1976). 1990. Vol. 15. № 11. P. 1175-1185.
/38.jpg)