Вступ
Фізіологічна кардія — це низка анатомічних утворень ділянки стравохідно-шлункового переходу, що забезпечують його замикально-клапанну функцію [1]. У формуванні замикальної функції кардії бере участь низка найважливіших механізмів: дещо підвищений тонус черевного відділу стравоходу (зона нижнього сфінктера стравоходу); більш високий (на 10 мм вод.ст.) тиск у цій частині стравоходу, ніж у шлунку; гострий кут Гіса (кут між стінкою стравоходу і дном шлунка) — чим він гостріший, тим потужнішим є клапанний ефект кардії; клапан Губарева, що являє собою складку слизової, утворену в місці переходу медіальної стінки стравоходу в медіальну стінку дна шлунка; газовий міхур шлунка, який підтримує функцію клапана Губарева; ніжки діафрагми (частіше медіальна), що утворюють м’язове кільце навколо стравоходу; ліва шлункова артерія, що частково фіксує абдомінальний і грудний відділи стравоходу; діафрагмально-стравохідна мембрана Лаймера — Бертеллі — серозна оболонка, що покриває та фіксує абдомінальний відділ стравоходу.
Неспроможність фізіологічної кардії — це стан, що супроводжується рефлюксом шлункового вмісту у стравохід — гастроезофагеальна рефлюксна хвороба (ГЕРХ), міграцією частини шлунка в грудну порожнину — грижі стравохідного отвору діафрагми (ГСОД).
ГСОД і ГЕРХ за поширеністю займають одне з провідних місць у сучасній гастроентерології та знаходяться у структурі захворювань шлунково-кишкового тракту на другому-третьому місцях, конкуруючи з такими захворюваннями, як хронічний холецистит і виразкова хвороба шлунка та дванадцятипалої кишки (ДПК) [2]. При цілеспрямованому обстеженні ГСОД виявляють у 1–9 %, а в осіб літнього віку — у 50 % спостережень [3]. ГСОД відіграють провідну роль у розвитку неспроможності кардії та патологічного шлунково-стравохідного рефлюксу [4]. ГСОД становить 98 % всіх гриж діафрагми, а у 50 % випадків не викликає ніяких клінічних проявів і не діагностується [5, 6]. ГСОД спостерігаються в 32,5–67,8 % випадків виразкової хвороби шлунка і ДПК, 52,5 % випадків хронічного гастродуоденіту, 15,8 % випадків хронічного панкреатиту, 4,5–53,8 % випадків хронічного холециститу. У виникненні рефлюксу із шлунка в стравохід відіграє велику роль ціла низка факторів: неспроможність нижнього стравохідного сфінктера (НСС); тимчасові епізоди розслаблення НСС; недостатність стравохідного кліренсу; патологічні зміни з боку шлунка, що підсилюють вираженість фізіологічного рефлюксу. Більш ніж у 85 % випадків епізоди зниження внутрішньостравохідної кислотності pH менше за 4 не супроводжуються будь-якими відчуттями [7].
Механізми утворення ГСОД складні і залежать від низки різних факторів. В патогенезі ГСОД вирішальну роль відіграють три групи факторів — послаблення сполучнотканинних структур (ослаблення зв’язкового апарату), підвищення внутрішньочеревного тиску, дискінезія травного тракту, зокрема стравоходу [8]. Набуті ГСОД розвиваються переважно у дорослих, що найчастіше пов’язано з інволюційними анатомічними змінами тканин, які утворюють стравохідний отвір.
Консервативна антирефлюксна терапія має симптоматичний характер, оскільки не усуває основні причини захворювання — ГСОД і недостатність фізіологічної кардії [9].
Основне завдання хірургічного лікування ГСОД — корекція анатомічних і фізіологічних порушень: усунення грижі, корекція антирефлюксной функції НСС, забезпечення вільного антеградного пасажу їжі [10–14]. Запропоновано багато способів виконання даних оперативних втручань і лапароскопічним, і відкритим доступом [10, 15]. Але, незважаючи на багаторічний досвід лапароскопічних втручань у хірургії ГСОД, багато питань залишаються актуальними і вимагають практичного вирішення [11, 16].
Ендохірургічна технологія у вигляді лапароскопічної фундоплікації (ЛФ), лапароскопічної хіатопластіки стрімко витісняє травматичну лапаротомічну технологію виконання даних втручань і по праву стає золотим стандартом.
Хірургічне лікування з приводу ГСОД включає такі етапи: виконання доступу; мобілізація езофагокардіального переходу; корекція розмірів стравохідного отвору діафрагми; збільшення протяжності і тиску НСС; фіксація НСС у черевній порожнині [17].
Велика кількість операцій (понад 60 запропонованих методик), що застосовуються при хірургічному лікуванні ГСОД та ГЕРХ, можна розділити на такі основні групи (рис. 1) [18].
Методика Nissen, при якій дно шлунка на 360° обертається навколо внутрішньочеревного відділу стравоходу у вигляді манжети, є найбільш надійною і тому найбільш часто використовується (рис. 1А) [19, 20, 22]. У клінічній практиці найчастіше застосовується модифікація фундоплікації за Nissen, описана S. Rohr і співавт. та відома в літературі як Floppy Nissen, при якій дно шлунка, на відміну від оригінальної методики, обертається у вигляді манжети довжиною всього 2 см, і модифікація Rosetti, коли манжетка формується в основному за рахунок передньої стінки шлунка [17, 21]. Рідше виконується фундоплікація за Toupet, при якій дно шлунка на 180° або 270° обертається навколо внутрішньочеревного відділу стравоходу по задній поверхні (рис. 1Б) [20–22].
Ще рідше проводиться операція за методикою Dor, при якій передню стінку фундального відділу шлунка укладають попереду абдомінального відділу стравоходу і фіксують до його правої стінки, при цьому перший шов обов’язково захоплює стравохідно-діафрагмальну зв’язку [25, 27]. З огляду на найнижчу антирефлюксну ефективність і часті рецидиви ГЕРХ фундоплікацію за Dor допустимо виконувати у випадках, коли виявляється виражений рубцевий або спайковий процес у просторі за стравоходом, який є технічною перешкодою для достатньої мобілізації шлунково-стравохідного переходу і виконання фундопликації за Nissen або Toupet. Таким чином, цей вид лапароскопічної фундоплікації є вимушеним і не використовується як самостійний спосіб корекції гастроезофагеального переходу в антирефлюксній хірургії (рис. 1В) [22–24].
Зазначені способи лікування хворих на ГСОД та ГЕРХ мають значні недоліки: при мобілізації фундального відділу шлунка виникає кровотеча; руйнуються діафрагмально-фундальна, діафрагмально-селезінкова, шлунково-селезінкова та шлунково-підшлункова зв’язки; новоутворена манжета, що обертає стравохід, розташовується нефізіологічно і може призводити до дисфагії; руйнується газовий міхур шлунка; кут Гіса; клапан Губарева; діафрагмальний компонент механізму замикання фізіологічної кардії; руйнується обмеження середостіння та абдомінального відділу стравоходу від черевної порожнини [30].
Серед ускладнень хірургічного лікування при застосуванні цих методик найбільше значення має рецидив ГСОД (10–84 %), зісковзування фундоплікаційної манжети (1–8 %), дисфагія (2–70 %), синдром gas-bloat (6–46 %) та відновлення печії (5–9 %) [28, 29].
Мета дослідження: підвищення ефективності хірургічного лікування неспроможності фізіологічної кардії при ГСОД шляхом розробки нового способу хірургічної корекції.
Матеріали та методи
У відділі хірургії органів травлення Державної установи «Інститут гастроентерології НАМН України» в 2020 році згідно з завданнями роботи проведено дослідження 56 хворих на ГСОД, із яких аксіальні ГСОД виявлені у 42 (75,0 %) (І тип), параезофагеальні ГСОД — у 6 (10,7 %) (ІІ тип), змішані ГСОД — у 8 (14,3 %) (ІІІ тип) (код за МКХ-10 — К44).
Пацієнтам проводили рентгенологічне дослідження стравоходу, шлунка, ДПК. Рентгенологічне дослідження полягало в оглядовій рентгеноскопії та рентгенографії стравоходу, шлунка, ДПК із застосуванням барію сульфату (код АТС VO8BF02) на апараті OPERA Т90SEX. Застосовувалися спеціальні методики і прийоми для виявлення недостатності стравохідно-шлункового переходу. Поліпозиційна рентгеноскопія проводилася у вертикальному, горизонтальному положенні хворого, в положенні Тренделенбурга, в момент підйому апарату, при форсованому диханні. Одним із основних інструментальних методів у дослідженні патології езофагогастродуоденальної зони була езофагогастродуоденоскопія, яку виконували у відділенні мініінвазивних ендоскопічних втручань та інструментальної діагностики інституту за допомогою фіброгастроскопа OLYMPUS GIF Q-20 (Японія) та відеогастроскопа PENTAX ЕG-290 Kp (Японія). Для дослідження моторної функції стравоходу і тиску на рівні НСС, а також контролю за станом сформованої фундоплікаційної манжети використовувалась манометрія. Дослідження виконуються з використанням оригінального пристрою для вивчення моторики шлунково-кишкового тракту МНХ-01 (захищений а.с. № 923521 «Пристрій для дослідження моторики біологічного об’єкта» і виготовлений компанією «Українські медичні системи»). Відбір хворих на лапароскопічну операцію здійснювали з урахуванням таких показань: діагноз грижі встановлений рентгенологічно і за даними ЕГДС з наявністю ускладнень (езофагіт, ерозії і виразки стравоходу, кровотечі), післяопераційний рецидив.
Результати та обговорення
Оперативні втручання, що були виконані обстеженим пацієнтам, наведені в таблиці 1.
Летальних випадків не відзначалось. У 2 хворих (3,6 %) виник пневмоторакс, у 2 (3,6 %) — кровотеча з капсули селезінки. Середня тривалість операції становила (135 ± 24) хв, середній час фіксації трансплантата — (24 ± 12) хв.
Ефективність проведеного лікування у хворих оцінювалася за такими критеріями: клінічне зникнення печії, відрижки, регургітації, болю в епігастрії; відсутність ерозій у нижній третині стравоходу, відсутність пролапсу слизової шлунка в стравохід за даними ЕГДС; відсутність пролабіювання частки шлунка в грудну порожнину, відсутність сфінктерної недостатності, відсутність пролапсу слизової шлунка за даними рентгенологічного дослідження; нормалізація тиску в НСС за даними манометрії.
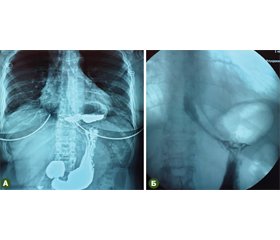
Під час вивчення віддалених результатів у 5 випадках (8,9 %) у віддалені терміни дослідження (до 6 міс.) діагностовані рецидиви ГСОД. У 2 (3,6 %) випадках причиною рецидиву були ознаки вкороченого стравоходу, що утруднювало накладання антирефлюксної манжети. В 1 (1,7 %) випадку фіксація алотрансплантату за ніжки діафрагми при великій ГСОД провокувалась прорізуванням швів. У 2 (3,6 %) випадках рецидив ГСОД був пов’язаний з технічними аспектами хірургічного лікування (рис. 2–6).
З метою поліпшення результатів лікування у хворих з ГСОД та ГЕРХ запропонований новий спосіб хірургічної корекції неспроможності фізіологічної кардії (рис. 7). За наявними літературними даними, такий спосіб оперативного втручання при ГЕРХ та ГСОД є невідомим.
Спосіб хірургічної корекції неспроможності фізіологічної кардії виконується наступним чином. На передній черевній стінці через проколи встановлюють 4 троакари, через які після накладання пневмоперитонеуму в черевну порожнину вводять інструменти. Проводять лапароскопічний огляд.
/56.jpg)
Виділяють з оточуючих тканин зі збереженням діафрагмально-фундальної, діафрагмально-селезінкової, шлунково-селезінкової та шлунково-підшлункової зв’язок тільки переднє півколо абдомінального відділу стравоходу та частину шлунка, яка знаходиться у грудній порожнині, і разом зі стравоходом максимально виводять у черевну порожнину. Виділяють медіальну і латеральну ніжки діафрагми. Виконують крурорафію накладанням одного П-подібного шва на праву стінку стравоходу на рівні кардії з фіксацією до неї обох ніжок діафрагми медіально від стравоходу (рис. 7А), використовуючи нитку зав’язаного П-подібного шва, накладають на медіальну ніжку діафрагми гофруючі шви, зменшуючи стравохідний отвір діафрагми до зовнішнього діаметра стравоходу (рис. 7Б). Накладають П-подібний шов на ліву стінку стравоходу на рівні кардії з фіксацією до неї латеральної ніжки діафрагми зліва від стравоходу та прилеглих до неї стінки фундального відділу шлунка і діафрагмально-фундальної зв’язки (рис. 7Б). Вводять шлунковий зонд у шлунок і перпендикулярно осі стравоходу виконують кардіогастроплікацію передньої стінки шлунка накладанням 2 П-подібних швів з подальшою гастродіафрагмопексією трьома швами (рис. 7В). Вколювання й виколювання голки при накладанні всіх швів здійснюються на відстані не менше 1,5 см (три діаметри голкозатискача) (рис. 7Г).
Перевагами способу є те, що лапароскопічне виділення тільки переднього півкола абдомінального відділу стравоходу та частини шлунка, яка знаходиться в грудній порожнині, з оточуючих зберігає діафрагмально-фундальну, діафрагмально-селезінкову, шлунково-селезінкову та шлунково-підшлункову зв’язки, що беруть участь у формуванні фізіологічної кардії, запобігає кровотечі з коротких артерій селезінки. Виконання крурорафії накладанням одного П-подібного шва на праву стінку стравоходу на рівні кардії з фіксацією до неї медіальної та латеральної ніжок діафрагми медіально від стравоходу та накладання гофруючих швів на медіальну ніжку діафрагми з використанням нитки зав’язаного П-подібного шва забезпечує зменшення стравохідного отвору діафрагми до зовнішнього діаметра стравоходу без подальшого залучення латеральної ніжки діафрагми, високе підшивання якої супроводжується утворенням «сходинки» для стравоходу та розвитком дисфагії.
Накладання П-подібних швів на праву і ліву стінку стравоходу на рівні кардії з фіксацією до неї латеральної ніжки діафрагми та прилеглих до неї стінки фундального відділу шлунка і діафрагмально-фундальної зв’язки забезпечує розташування зони стравохідно-шлункового переходу в черевній порожнині, відновлює кут Гіса і газовий міхур шлунка, посилює заднє півколо нижнього сфінктера стравоходу, виконання перпендикулярно осі стравоходу кардіогастроплікації передньої стінки шлунка накладанням П-подібних швів, відновлює клапан Губарева і посилює переднє півколо нижнього сфінктера стравоходу, а гастродіафрагмопексія забезпечує відновлення діафрагмального компонента механізму замикання фізіологічної кардії і здійснює обмеження середостіння й абдомінального відділу стравоходу від черевної порожнини.
Клінічний приклад 1. Хворий Ф., 1968 року народження, медична карта № 1743, перебував на стаціонарному лікуванні у відділенні хірургії органів травлення інституту з 16.11.2020 по 24.11.2020. Основний діагноз: гастроезофагеальна рефлюксна хвороба, рефрактерна.
Анамнез хвороби: вважає себе хворим з початку 2018 року, коли з’явились скарги на стійку печію, дискомфорт в епігастрії. Неодноразово проходив консервативне лікування з застосуванням інгібіторів протонної помпи, альгінатів та ін. з короткочасним позитивним ефектом. З червня 2020 року скарги посилилися. Надійшов на обстеження та оперативне лікування.
Відеоезофагогастродуоденоскопія (17.11.2020). Стравохід: стравохідно-шлункове з’єднання (EGJ) на 40 см від різців, Z-лінія на 40 см, чітка, хіатус на 43 см. CLE — немає. Нижній стравохідний сфінктер не змикається (в ретрофлексії — кардіальна складка 3 ступеню). Палісадні судини визначаються, збігаються з Z-лінією. Слизова стравоходу рожева, в дистальному відділі потовщена, гіперемована, з ерозіями діаметром до 2 мм. Шлунок: в шлунку — помірна кількість прозорої рідини. Слизова оболонка шлунка складчаста, еластична, у верхніх відділах рожева, в антральному відділі дрібноплямиста, з сегментами гіперемії та поодинокими ерозіями і сегментами атрофії. Воротар: змикається. ДПК: слизова цибулини гіперемована, з множинними геморагіями, в просвіті жовч, в позацибулинному відділі слизова рожева, рівномірна, в просвіті жовч. Великий дуоденальний сосочок без змін. Виконана манометрія. Висновок: еритематозно-геморагічна бульбопатія. Ерозивно-еритематозна гастропатія (антрум) з ознаками атрофії. Недостатність кардії. Ерозивний рефлюкс-езофагіт. Уреазний тест — негативний.
Манометрія (17.11.2020). Значення вимірювання: тиск у нижньому стравохідному сфінктері дорівнював 13,61 мм рт.ст. Тиск у пілоричному сфінктері дорівнював 24,25 мм рт.ст. (норма тиску дорівнює 10–15 мм рт.ст.).
Рентгенологічне дослідження від 18.11.2020. Стравохід прохідний. Шлунок — контури чіткі, перистальтика збережена по обом кривизнам. Цибулина ДПК чітка. Пасаж барію не порушений. При спеціальних методах дослідження (положення Тренделенбурга) спостерігається виражений закид барію з шлунка в нижню третину стравоходу. Висновок: гастроезофагеальний рефлюкс.
Протокол операції № 269 від 19.11.2020 р. Назва операції: лапароскопія. Езофагокрурорафія. Гастроплікація. Гастродіафрагмопексія.
Перебіг післяопераційного періоду гладкий. Клінічно при прийомі їжі та вночі під час сну скарг на печію та кашель не пред’являє.
Рентгенологічне дослідження з контрастною речовиною від 23.11.2020: розташування газового міхура шлунка відмічається в типовому місті, кут Гіса становить 45°. При спеціальних методах дослідження — без ознак гастроезофагеального рефлюксу порівняно з даними від 18.11.2020 (рис. 8).
Клінічний приклад 2. Хвора К., 29.10.1984 року народження, медична карта № 1616, перебувала на стаціонарному лікуванні у відділенні хірургії органів травлення інституту з 21.10.2020 по 04.11.2020. Основний діагноз: грижа стравохідного отвору діафрагми.
Анамнез хвороби: вважає себе хворою з 2015 року, коли з’явились скарги на стійку печію, нічний кашель, що спонукав спати в положенні напівсидячи, нудоту, що виникала після споживання кислої їжі та при нахилі тулуба вниз, біль за грудиною. Неодноразово проходила консервативне лікування з застосуванням інгібіторів протонної помпи, альгінатів та ін., однак з позитивним ефектом лише на час прийому. З жовтня 2020 року скарги посилилися. Надійшла на обстеження та оперативне лікування.
Відеоезофагогастродуоденоскопія (19.10.2020). Стравохід: стравохідно-шлункове з’єднання (EGJ) на 39 см від різців, Z-лінія на 38 см, чітка, хіатус на 42 см. CLE — немає. Нижній стравохідний сфінктер не змикається (в ретрофлексії — кардіальна складка 3 ступеня). Палісадні судини визначаються, збігаються з Z-лінією. Слизова стравоходу рожева, дещо потовщена. В режимі NBI мікросудинний рисунок правильний. Визначається гастроезофагеальний рефлюкс і пролапс слизової шлунка в стравохід. Шлунок: в шлунку помірна кількість мутної рідини з домішками жовчі. Слизова оболонка шлунка складчаста, еластична, в верхніх відділах рожева, в антральному відділі дрібноплямиста, з полями помірної атрофії. В режимі NBI мікросудинний рисунок правильний. Воротар: змикається не повністю. ДПК: слизова цибулини рожева, у просвіті жовч, в позацибулинному відділі слизова рожева, рівномірна, у просвіті жовч. Великий дуоденальний сосочок поліпоподібний, розміром до 3 мм, слизова рожева. В режимі NBI мікросудинний рисунок правильний. Висновок: гастропатія (антрум) з ознаками помірної атрофії. Дуоденогастральний рефлюкс. Недостатність кардії. Ознаки грижі стравохідного отвору діафрагми. Уреазний тест негативний.
Манометрія (19.10.2020). Значення вимірювання: тиск у нижньому стравохідному сфінктері дорівнював 0,21 мм рт.ст. Тиск у пілоричному сфінктері дорівнював 10,60 мм рт.ст. (норма тиску — 10–15 мм рт.ст.).
Рентгенологічне дослідження від 07.10.2020. Стравохід прохідний. Шлунок у верхньому відділі утворює згин до спини, перистальтика збережена по обом кривизнам. Цибулина ДПК чітка. Пасаж барію не порушений. При спеціальних методах дослідження (положення Тренделенбурга) відмічається пролабування кардії в грудну порожнину розміром 4,4 × 3,0 см. Висновок: параезофагеальна грижа стравохідного отвору діафрагми.
Оперативне лікування. Протокол операції № 240 від 28.10.2020 р. Назва операції: лапароскопія. Езофагокрурорафія. Гастроплікація. Гастродіафрагмопексія.
Перебіг післяопераційного періоду гладкий. Клінічно зранку та при прийомі їжі скарг на нудоту і блювання не пред’являє.
Рентгенологічне дослідження з барієм від 02.11.2020: розташування газового міхура шлунка відмічається в типовому місті, кут Гіса становить 45°. В положенні лежачи на животі — без ознак гастроезофагеального рефлюксу. При спеціальних методах дослідження (положення Тренделенбурга) грижі стравохідного отвору діафрагми не виявлено порівняно з даними від 07.10.2020 (рис. 9).
Запропонованим способом проведено лікування в 11 хворих, післяопераційний стан пацієнтів був задовільний, без ознак післяопераційних дисфагічних розладів. В усіх випадках отримані хороші безпосередні та віддалені результати терміном від 6 місяців до 1 року.
Висновки
Таким чином, запропонований спосіб хірургічного лікування неспроможності фізіологічної кардії при ГСОД є менш травматичним, ніж відомі. Застосування запропонованого способу забезпечує надійне відновлення фізіологічної кардії та збереження анатомічних відношень діафрагми і зони стравохідно-шлункового переходу, зменшує ризик виникнення кровотечі, гіперфункції кардії. В післяопераційному періоді даний спосіб хірургічного лікування зменшує ймовірність розвитку рецидиву неспроможності фізіологічної кардії, виникнення дисфагії та рецидиву захворювання.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Інформація про фінансування. Робота виконується відповідно до плану наукових досліджень відділу хірургії органів травлення Державної установи «Інститут гастроентерології НАМН України». Усі пацієнти підписали інформовану згоду на участь у цьому дослідженні.
Внесок авторів: Шевченко Б.Ф. — концепція та дизайн дослідження, редагування тексту; Пролом Н.В., Бабій О.М. — відбір пацієнтів, обробка клінічних і статистичних даних, написання статті; Зеленюк О.В. — збір та обробка матеріалу, статистична обробка; Тарабаров С.О. — виконання ендоскопічних досліджень з манометрією і аналіз отриманих результатів.
Отримано/Received 16.02.2021
Рецензовано/Revised 02.03.2021
Прийнято до друку/Accepted 12.03.2021
/53.jpg)

/52.jpg)
/54.jpg)
/55.jpg)
/56.jpg)
/57.jpg)
/58.jpg)