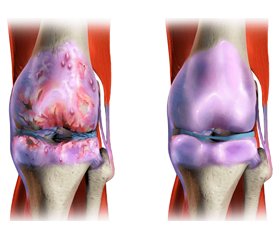
Остеоартроз (ОА) відноситься до дегенеративних захворювань, при яких частіше вражаються кульшові та колінні суглоби. ОА характеризується деструктивними й гіперпластичними змінами суглобних кінців кісток і проявляється болем, дефігурацією суглобів й прогресуванням порушення їх функції [7].
Згідно з епідеміологічними дослідженнями, на частку ОА припадає 10–12 % усіх випадків захворювань опорно-рухового апарату. Серед суглобної патології ОА становить 60–80 % [3], з віком частота хвороби збільшується. У загальній структурі патології коліна захворювання на нього становлять 57,8 % від загальної кількості патологій колінного суглоба.
Актуальність проблем гонартрозу (ГА) обумовлена не тільки його поширеністю, але й високим ризиком розвитку обмежень функції колінних суглобів, що супроводжується значним зниженням якості життя пацієнтів і нерідко призводить до часткового порушення працездатності або стійкої інвалідизації хворих [1, 23]. За даними Н.И. Трофимовича [11], питома вага стійкої втрати працездатності через захворювання суглобів становить до 30 %, серед них 14,6 % випадків припадає на остеоартроз колінних суглобів зі стійким негативним прогнозом перебігу. Серед осіб віком понад 50 років ОА відзначається у 27 % випадків, а понад 65 — у 97 %.
ГА має значні гендерні особливості перебігу [10], з якими пов’язані тяжкість, темпи прогресування захворювання й поширеність артикулярного патологічного процесу. У чоловіків частіше реєструються кісти Бейкера, трабекулярний набряк у виростках стегнової і великогомілкової кісток, лігаментоз, зміни передньої хрестоподібної зв’язки, перилігаментіт, а в жінок — субхондральний склероз, зміни заднього рогу медіального меніска, остеокістоз та внутрішньосуглобові тіла Гоффа. Частка жінок, які страждають від ГА, становить близько 70 % хворих на первинний ОА [24, 31]. Популяційними дослідженнями було встановлено ГА у 15 % загальної популяції жінок, тоді як у чоловіків того ж віку захворювання відмічалося майже у 2 рази рідше [37], але, за іншими даними, частота ГА у чоловіків до 60 років вища, а у жінок вона починає зростати після 65 років [27].
Вважається, що остеоартроз є віковою хворобою, але останніми роками він спостерігається і в людей молодого віку. Все частіше дослідники спостерігають ознаки гонартрозу у молодих працездатних людей [6, 12], у тому числі спортсменів [32]. Відмічається, що 58 % хворих на ГА, які перенесли ендопротезування, були молодше 60 років [5].
Остеоартроз колінного суглоба. Перебіг захворювання. Залежно від обсягу ураження тканин суглоба виділяють 4 стадії артрозу колінного суглоба, визначаючи його симптоми [16]:
— І — симптоми відсутні, але при рентгенологічному обстеженні виявляються незначні відхилення від норм — потоншення хряща. Біль проявляє себе у вигляді легкого дискомфорту при підйомі сходами, потім поступово наростає; ранкова скутість починається з декількох хвилин і поступово наростає;
— ІІ — пацієнт відмічає епізодичні болі при фізичних навантаженнях, при ходьбі сходами, присіданнях, довгому перебуванні у стоячому положенні; на знімках виявляються звуження суглобної щілини, ознаки дегенерації; початкові прояви остеофітів або кальцифікації латеральних зв’язок суглоба. З’являється хруст, який відрізняється від фізіологічного звуку різкістю та особливою тональністю, а також супроводжує больовими відчуттями, починається формування тугорухомості;
— ІІІ — біль постійний, навіть у спокої, ходіння без тростини неможливе; на рентгенівських знімках видно значне звуження суглобної щілини, іноді асиметричне через пошкодження менісків, ознаки деформації суглоба, остеофіти, кісткові розростання. Згинання та розгинання коліна утруднене і часто супроводжується болем. Формується деформація коліна, яка виникає через зміну форм кісток суглоба, кісткових розростань та залучення у патологічний процес м’язів і зв’язок, приєднуються запалення та набряк тканин, прогресує кульгавість;
— IV — рух у суглобах практично неможливий, рентгенологічно виявляється повне руйнування хряща і значна деформація суглобних поверхонь, велика кількість остеофітів. У тяжких випадках кістки зростаються між собою, на останніх стадіях існування суглоб може повністю заблокуватися (анкілоз).
Ендопротезування займає провідне місце у лікуванні ІІІ–IV стадій остеоартрозу колінного суглоба. Головні атрибути тотального ендопротезування (ТЕП) — рухомість, стабільність і безболісність, що є перевагою перед іншими традиційними методами лікування суглоба: медикаментозний, що може допомогти тільки на ранніх стадіях остеоартрозу, чи артродез, що усуває біль, але позбавляє суглоб рухливості.
Отже, показанням до ендопротезування колінного суглоба при дегенеративних захворюваннях є артрози й артрити в стадії повного руйнування та асептичні некрози.
Протипоказання до ендопротезування можна поділити на абсолютні і відносні. Абсолютні — це ті, що усунути неможливо.
До протипоказань зараховують: декомпенсовані захворювання серця, легень, нирок, ендокринні захворювання; психічні розлади; порушення рухової функції; наявність гнійних захворювань.
Ускладнення ендопротезування колінного суглоба. Тенденція до збільшення загальної кількості операцій та зменшення віку пацієнтів, яким проводять ендопротезування колінного суглоба, призводить до збільшення частоти ускладнень та незадовільних результатів. За даними деяких авторів, на результати ендопротезування скаржаться від 3,3 до 13,2 % хворих, інфекційні ускладнення розвиваються в 0,5–3,5 % випадків, при цьому частка повторних втручань становить 3,2–5,6 % [25, 28].
Параартикулярний біль, контрактури, асептична нестабільність компонентів ендопротеза зустрічаються в 3–12 % випадків [9].
За даними об’єднаних національних реєстрів ТЕП колінного суглоба, до 18,2 % пацієнтів незадоволені результатом операції, як правило, через біль [8, 17].
Серед основних чинників, що призводять до виникнення ускладнень ТЕП колінного суглоба, виділяються ускладнення, пов’язані з самим оперативним втручанням (40 % загальної кількості), серед них на частку помилок під час встановлення ендопротеза припадає 80 % випадків, на інші 20 % припадали випадки, коли протезування можна було замінити іншими видами лікування. Ускладнення, пов’язані з самим пацієнтом, становили 20 % загальної кількості [2, 26].
Особливості відновлення хворих після ТЕП колінного суглоба. У 2017 році J. Naili et al. [30] провели дослідження щодо скарг хворих у віддалені періоди після ТЕП колінного суглоба та порівняли результати інструментальних досліджень хворих, які повідомляли про добрі результати щодо якості життя, покращили біомеханіку колінного суглоба при ходьбі, з результатами хворих, які скаржилися на погані результати. Отже, незважаючи на зменшення болю в усіх хворих, у хворих, які оцінювали результат лікування як хороший, значно покращили біомеханіку ходьби, у них збільшився діапазон згинання/розгинання коліна, зменшився пік варусного кута, збільшилася швидкість пересування. У хворих, які відмічали поганий результат, спостерігали збільшення варусного кута при згинанні коліна при ходьбі та не відмічали помітного покращення параметрів ходьби порівняно з доопераційним дослідженням.
Колективом дослідників B. Alice et al. (2015) [13] було визначено, що через 3 місяці після операції ТЕП колінного суглоба пацієнти завжди ходять повільніше, швидкість згинання/розгинання суглоба значно менша, ніж в контрольній групі. Але спостерігається де-який прогрес щодо збільшення довжини кроку, швидкості ходьби та фронтального вирівнювання колінного суглоба порівняно з доопераційним обстеженням.
Більш ретельне дослідження ходьби хворих та ступінь покращення біомеханіки ходьби після ендопротезування колінного суглоба провели дослідники Школи реабілітаційної науки Шанхайського університету традиційної китайської медицини. За даними W. Xubo et al. (2017) [40], проведене 3D-дослідження ходьби 18 хворих після ТЕП колінного суглоба показало, що оперований бік демонструє значно менший загальний час підтримки та час одноразової підтримки, а також значно довшу фазу маху порівняно з іншим боком. Під час ходьби оперований бік мав значно менший кут згинання колінного суглоба під час розмаху та більший кут згинання коліна й вальгусний кут під час середньої фази кроку (одноопорна фаза кроку), ніж неоперований бік. Була помірна та значна кореляція між характером ходьби та динамічною кінематикою коліна. Отже, дослідники визначили, що після ТЕП колінного суглоба порушення ходьби були пов’язані з неадекватним згинанням колін у фазі розмаху та недостатнім розгинанням у фазі стояння, а також збільшенням діапазону вальгуса.
Ці ж дослідники [38] пізніше показали, що між просторово-часовими параметрами оперованого боку ноги та оцінкою WOMAC під час ходьби існує помірна негативна кореляція, висока кореляція між оцінкою WOMAC та піковим згинанням коліна при махах, кутом згинання коліна й кутом вальгуса в середній стійці, за винятком довжини кроку та швидкості руху вперед, інші параметри ходьби суттєво корелювали з показником якості життя SF-36. За результатами досліджень було визначено, що означені вище параметри просторової орієнтації колінного суглоба при ходьбі у ранні терміни після операції можуть використовуватися як ефективні показники для оцінки післяопераційної функції коліна та ефективності реабілітації якості життя після операції ендопротезування колінного суглоба.
Після одностороннього ТЕП колінного суглоба схеми навантаження фронтальної площини на опероване коліно залишаються патологічними в довгостроковій перспективі. Група дослідників E.M. Debbi (2015) [21] припустила, що неопероване коліно має більші навантаження на фронтальну площину після операції, отже, завданням цього дослідження було порівняти передопераційну та ранню післяопераційну схеми навантаження обох колін після одностороннього ТЕП колінного суглоба. Було визначено, що у фронтальній площині ТЕП колінного суглоба зменшує навантаження на оперованому коліні та не погіршує навантаження в неоперованому, отже, терапія після операції повинна бути зосереджена на збереженні зменшення моменту аддукції в оперованому суглобі та запобіганні подальшому погіршенню структури навантаження в неоперованому.
Відомо, що після операції ТЕП колінного суглоба серед пацієнтів відмічають м’язову слабкість. M.M. Ardestani і M. Moazen (2016) [15] проаналізували роботу м’язів і колінних суглобів при різних м’язових порушеннях та визначили мінімальні вимоги до м’язової сили, необхідні для збереження моделей ходьби після ТЕП колінного суглоба. Моделювання й аналіз проводили з використанням статистичного підходу для оцінки форм хвилі ходьби, тобто просторового відображення параметрів ходьби. Результати цього дослідження містять клінічно важливі, хоча й попередні пропозиції: м’язи згиначів стегна та підошовного згинача компенсували слабкість розгиначів стегна; розгиначі тазостегнових суглобів, аддукторів стегна та підошовно-згинальних м’язів гомілковостопного суглоба компенсували слабкості згиначів стегна; м’язи згиначів стегна та коліна реагували на слабкість згиначів стегна; слабкість розгиначів коліна та згиначів коліна компенсувалась м’язами розгиначів і розгиначів стегна.
K.L. Paterson et al. (2017, 2018, 2020) провели тривале дослідження щодо впливу статі та маси тіла (ожиріння) на результати ТЕП колінного суглоба при остеоартрозі. Дослідники вивчали просторові показники ходьби хворих до [33] ТЕП колінного суглоба, що планується, і через 6 місяців та 2 роки. До ендопротезування було визначено, що у чоловіків більш високий абсолютний пік моменту аддукції коліна та вертикальної сили на опору порівняно з жінками, різниця між статями залишалася після коригування на розмір тіла. Біомеханіка колін була близькою в групах ожиріння, група ожиріння не впливала на кінематику або моменти колінного суглоба.
Через 6 місяців після ТЕП колінного суглоба були проаналізовані результати у тих же хворих [34]. Було визначено, що стать, а не ожиріння впливає на зміну біомеханіки ходьби після артропластики. У чоловіків після операцій зберігається ненормальна ходьба, а у жінок ходьба покращується.
Віддалені результати через 2 роки після ТЕП колінного суглоба [35] підтвердили, що на зміну біомеханіки ходьби впливає стать, а не ожиріння. Через 2 роки у чоловіків спостерігався більший варусний кут при ходьбі, більш низький піковий кут у фронтальній площині коліна. Але біомеханіка ходьби через 2 роки не відрізнялася між групами з доопераційним ожирінням та без нього.
Близькі дані отримали дослідники A. Phinyomark et al. (2016) [36], жінки з ОА та здорові показали значущо більші кути відведення колінного суглоба та стегна порівняно з чоловіками тих же груп. При дослідженні параметрів ходьби з точністю 98–100 % була знайдена різниця між гендерними група. Ці результати, на думку авторів, передбачають, що при дослідженні біомеханічної етіології ОА колінного суглоба треба враховувати стать, а також розробити протоколи аналізу та реабілітації з урахуванням гендерного фактора.
Результатом численних досліджень ходьби хворих після ТЕП колінного суглоба можна вважати висновок, зроблений дослідниками M. Aljehani et al. (2019) [14]. Однобічні симптоми та однобічне ТЕП колінного суглоба відмічаються частіше, у багатьох пацієнтів спостерігається двосторонній рентгенологічний ОА. Оскільки протилежна (неоперована) кінцівка часто використовується для порівняння клінічних і біомеханічних результатів, важливо вважати, що наявність ОА впливає на схеми руху в будь-якій кінцівці. На двох групах хворих (з однобічним та двобічним ОА) після одностороннього ТЕП колінного суглоба були порівняні параметри ходьби через 6 та 24 місяці після лікування. Визначено, що хворі з контралатеральним ОА коліна, мають більш симетричну ходьбу, хоча спостерігаються порушення з обох боків. У хворих з однобічним ОА було виявлено більше різниці між параметрами кроку. На думку авторів, симетричні схеми рухів між кінцівками після операції не повинні бути єдиним фактором, на якому базується відновлення руху, слід враховувати стан контралатерального колінного суглоба.
Майбутнє хірургії тотального ендопротезування колінного суглоба включатиме планування, що залучає більш специфічні для пацієнта характеристики. Незважаючи на відомі біологічні, морфологічні та функціональні відмінності між чоловіками й жінками, мало досліджено біомеханічних і нервово-м’язових відмінностей колінного суглоба між чоловіками та жінками з ОА, не вивчалися біомеханічні та нервово-м’язові реакції, специфічні для статі, на операцію ТЕП. J.L. Astephen Wilson et al. (2015) [39] вивчали пов’язані зі статтю різниці в кінематиці та нервово-м’язових патернах колінного суглоба при ходьбі до та через 1 рік після ТЕП. Було виявлено низку специфічних для статі відмінностей, які дозволяють припустити різний прояв кінцевої стадії ОА коліна між статями.
Реабілітація. Особливості та складнощі. За класичними даними ведення хворих на остеоартроз колінного суглоба, реабілітаційні заходи починають ще до операції ендопротезування. Основними лікувальними процедурами є фізіотерапевтичні. Фізіотерапія — важлива частина реабілітації після ТЕП, але вплив доопераційної фізіотерапії вивчено мало. У 2015 році дослідниками Каледонського університету (Глазго) було проведено систематизований пошук літературних даних щодо рандомізованих конт-
рольованих досліджень (з 2004 по 2014 р.) щодо впливу передопераційної фізіотерапії на результати ТЕП колінного суглоба у пацієнтів похилого віку [20]. Дослідники визначили, що недостатньо доказів того, що предопераційна фізіотерапія більш ефективна, ніж її відсутність або звичайний догляд.
Аналогічних висновків дійшли дослідники малайзійської ортопедичної школи, які у 2016 році провели широке рандомізоване дослідження щодо передопераційної фізіотерапії. За їх даними, 6-тижнева доопераційна фізіотерапія не показала значного впливу на короткочасні функціональні результати після первинного ТЕП колінного суглоба [29].
Після операції ендопротезування в комплекс реабілітаційних заходів включають фізичні вправи, що направлені на відновлення м’язової сили і на вироблення правильної ходьби. Отже, вивчення порушень, що відбуваються під час перебігу ОА, дають можливість правильно сформувати лікувальні вправи на усунення сформованих патологічних звичок ходьби.
Групою реабілітологів було проведено дослідження щодо програми відновлення навичок ходьби у хворих після ТЕП колінного суглоба. Вивчали найближчі та довгострокові наслідки програми навичок ходьби порівняно із звичайною фізіотерапією на фізичну функцію, біль та сприйняття самоефективності. На результатах лікувальної фізкультури (ЛФК) 57 пацієнтів було визначено, що програма навичок ходьби мала кращий вплив на ходьбу, ніж звичайна фізіотерапія. Реабілітація, що зосереджена на вивченні різних способів ходьби через практику, дає більш помітні результати у пацієнтів після ендопротезування колінного суглоба [18].
Для відновлення повноцінної ходьби важливі не тільки корекція кутів згинання суглобів нижніх кінцівок, довжина та тривалість кроків, важливу роль відіграють динамічні параметри всього тіла.
Рух тулуба є важливим, але ще мало вивченим після повного ендопротезування коліна. Група японських вчених [19] аналізувала періодичність руху тулуба (кут, швидкість та зміщення), параметри кроків, швидкість ходьби (довжина кроку, ширина кроку) та діапазон рухів суглобів нижніх кінцівок (стегна, коліна та гомілковостопний суглоб) для подальшого використання отриманих даних в програмі післяопераційної реабілітації після ендопротезування. Було визначено, що максимальна швидкість тулуба була направлена у бік, контралатеральний протезованому, максимальне зміщення тулуба у бік протезування було зменшеним, максимальна швидкість вгору на боці протезування збільшилася, а максимальне зміщення тулуба на боці, протилежному протезуванню, значно зменшилося у напрямку вгору-вниз. Відновлення приведення стегна під час фази стояння поліпшує вирівнювання колін, сприяє зменшенню руху тулуба в оперований бік. У ранній період після ендопротезування зменшення руху стовбура в коронарній площині є корисним для підтримання балансу стовбура та запобігання падінням.
Після виписки зі стаціонару та проходження первинної реабілітації необхідна подальша післяопераційна ЛФК для підтримання функціональної рухливості суглобів. Телереабілітація може бути потенційним інноваційним підходом до лікування. Німецькими вченими [22] у 2017 році була запропонована та зареєстрована програма телереабілітації 110 учасників після ТЕП колінного або кульшового суглобів. Планується, за програмою, провести 3-місячне інтерактивне домашнє тренування з використанням телереабілітації. Очікується, що учасники отримують користь від програми за всіма показниками, і в разі успіху ця система може бути застосована в широкого кола хворих.
Функціональне відновлення нижніх кінцівок є тривалим процесом, і необхідне стійке функціональне тренування.
Висновки
Огляд літератури показав, що при тяжких дегенеративних ураженнях колінного суглоба у хворих порушується біомеханіка руху, що може призвести до інвалідності.
Ендопротезування колінного суглоба позбавляє хворого болю, покращує якість життя, але, за даними багатьох дослідників, хворі скаржаться на неповне відновлення функціональності протезованої кінцівки. За результатами аналізу дослідників, основними причинами неповного відновлення параметрів ходьби є різниця у фронтальних кутах згинання колінного суглоба й різниця у довжині кроків. Спеціальні тренувальні вправи дозволяють зменшити несиметричність кроків, але повністю відновити симетричність кроків у термін до 2 років складно.
Проведені дослідження впливу доопераційної реабілітації на результат ендопротезування колінного суглоба показали її малу ефективність.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 27.04.2021
Рецензовано/Revised 11.05.2021
Прийнято до друку/Accepted 17.05.2021
Список литературы
1. Борткевич О.П. Сучасні інструментальні методи візуалізації в ревматології: Магнітно-резонансна томографія. Український ревматологічний журнал. 2007. 28(2). 10-16.
2. Гайко Г.В., Сулима О.М., Торчинський В.П., Підгаєцький В.М., Осадчук Т.І. Помилки та ускладнення тотального ендопротезування колінного суглоба. Вісник ортопедії, травматології та протезування. 2019. 4. 4-10. DOI: 10.37647/0132-2486-2019-103-4-4-10.
3. Губачев Ю.М., Макиенко В.В. Болезни суставов. СПб., 1998.
4. Коваленко В.М., Борткевич О.П. Застосування МРТ и УЗД в діагностиці остеоартрозу. Український ревматологічний журнал. 2010. 39(1). 55-86.
5. Колесников М.А. Лечение гонартроза: современные принципы и подходы. Практическая медицина. 2010. 8(47). 97-99.
6. Лебець І.С., Шевченко Н.С., Матвієнко О.В., Неліна І.М. Механізми формування остеоартрозу в підлітків. Український ревматологічний журнал. 2007. 30(4). 3-6.
7. Михайлов А.Н. Руководство по медицинской визуализации. Мн.: Выш. школа, 1996.
8. Паратте С., Корнилов Н.Н., Тиенпонт Э., Балдини А., Тихилов Р.М., Аргенсон Ж.-Н., Куляба Т.А. Необъяснимая боль после тотального эндопротезирования коленного сустава. Травматология и ортопедия России. 2013. 4(70). 92-6. doi: 10.21823/2311-2905-2013-4-92-96.
9. Румянцев Ю.И. Лучевая диагностика осложнений эндопротезирования тазобедренного и коленного суставов. Бюллетень сибирской медицины. 2012. 11(5). 5.
10. Синяченко О.В., Єрмолаєва М.В., Ютовец Т.С., Головкина Е.С. Гендерно-вікові особливості перебігу гонартрозу. Український ревматологічний журнал. 2013. 51(1). 33-37.
11. Трофимович Н.И. Медико-социальная экспертиза при дегенеративно-дистрофических поражениях коленного сустава. Здравоохранение (Белоруссия). 1999. 2. 27-29.
12. Шевченко Н.С., Лебец И.С., Нелина И.Н., Кашкалда Д.А. Патогенетическая значимость воспаления при остеоартрозе у подростков с инициальными стадиями заболевания. Український ревматологічний журнал. 2010. 39(1). 50-54.
13. Alice B., Stéphane A., Yoshisama S., Pierre H., Domi-zio S., Hermes M., Katia T. Evolution of knee kinematics three months after total knee replacement. Gait Posture. 2015. 41(2). 624-9. doi: 10.1016/j.gaitpost.2015.01.010 [Epub 2015 Jan 19].
14. Aljehani M., Madara K., Snyder-Mackler L., Christiansen C., Zeni J.A. Jr. The contralateral knee may not be a valid control for biomechanical outcomes after unilateral total knee arthroplasty. Gait Posture. 2019. 70. 179-184. doi: 10.1016/j.gaitpost.2019.01.030.
15. Ardestani M.M., Moazen M. How human gait responds to muscle impairment in total knee arthroplasty patients: Muscular compensations and articular perturbations. J. Biomech. 2016. 49(9). 1620-1633. doi: 10.1016/j.jbiomech.2016.03.047.
16. Aweid O., Haider Z., Saed A., Kalairajah Y. Treatment modalities for hip and knee osteoarthritis: A systematic review of safety. Journal of Orthopaedic Surgery. 2018 Nov 8. 26(3). doi: 10.1177/2309499018808669.
17. Brander V.A., Stulberg S.D., Adams A.D., Harden R.N., Bruehl S., Stanos S.P., Houle T. Ranawat Award Paper: Predicting Total Knee Replacement Pain (A Prospective, Observational Study). Clinical Orthopaedics and Related Research. 2003. 416. 27-36. doi: 10.1097/01.blo.0000092983.12414.e9.
18. Bruun-Olsen V., Heiberg K.E., Wahl A.K., Mengshoel A.M. The immediate and long-term effects of a walking-skill program compared to usual physiotherapy care in patients who have undergone total knee arthroplasty (TKA): a randomized controlled trial. 2013. 35(23). 2008-2015. doi: 10.3109/09638288.2013.770084.
19. Chang Q.Z., Sohmiya M., Wada N., Tazawa M., Sato N., Yanagisawa S., Shirakura K. Alternation of trunk movement after arthroplasty in patients with osteoarthritis of the knee. J. Orthop. Sci. 2011. 16(4). 382-8. doi: 10.1007/s00776-011-0066-y.
20. Chesham R.A., Shanmugam S. Does preoperative phy-siotherapy improve postoperative, patient-based outcomes in older adults who have undergone total knee arthroplasty? A systematic review; Physiother. Theory Pract. 2017. 33(1). 9-30. doi: 10.1080/09593985.2016.1230660.
21. Debbi E.M., Bernfeld B., Herman A., Laufer Y., Greental A., Sigal A., Zaulan Y., Salai M., Haim A., Wolf A. Frontal plane biomechanics of the operated and non-operated knees before and after unilateral total knee arthroplasty. Clin. Biomech. (Bristol, Avon). 2015. 30(9). 889-94. doi: 10.1016/j.clinbiomech.2015.07.013.
22. Eichler S., Rabe S., Salzwedel A., Müller S., Stoll J., Tilgner N., John M., Wegscheider K., Mayer F., Völler H. Effectiveness of an interactive telerehabilitation system with home-based exercise training in patients after total hip or knee replacement: Study protocol for a multicenter, superiority, no-blinded randomized controlled trial. Randomized Controlled Trial. Trials. 2017. 18(1). 438. doi: 10.1186/s13063-017-2173-3.
23. Felson D.T. Osteoarthritis: Virtual joint replacement as an outcome measure in OA. Nat. Rev. Rheumatol. 2012. 8(4). 187-188.
24. Hawker G.A., Badley E.M., Croxford R., Coyte P.C. A population-based nested case-control study of the costs of hip and knee replacement surgery. Med. Care. 2009. 47(7). 732-741.
25. Indelli P.F., Glori G., Maloney W. Level of constraint in revision knee arthroplasty. Curr. Rev. Musculoskelet. Med. 2015. 8(4). 390-397.
26. Kellgren J. Lawrence J. Radiological assessment of osteoarthritis. Ann. Rheum. Dis. 1957. 16. 494-501.
27. Lacey R.J., Thomas E., Duncan R.C., Peat G. Gender difference in symptomatic radiographic knee osteoarthritis in the knee clinical assessment — CAS (K): a prospective study in the general population. BMC Musculoskelet. Disord. 2008. 11(9). 82-83.
28. Lentino J.R. Prosthetic joint infections: bane of orthopedists, challenge for infectious disease specialists. Clin. Infect. Dis. 2003. 36. 1157-1161.
29. Mat Eil Ismail M.S., Sharifudin M.A., Shokri A.A., Ab Rahman S. Preoperative physiotherapy and short-term functional outcomes of primary total knee arthroplasty. Randomized Controlled Trial. Singapore Med. J. 2016. 57(3). 138-43. doi: 10.11622/smedj.2016055.
30. Naili J., Wretenberg P., Lindgren V., Iversen M., Hedström M., Broström E. Improved knee biomechanics among patients reporting a good outcome in knee-related quality of life one year after total knee arthroplasty. BMC Musculoskelet. Di-sord. 2017. 18(1). 122. doi: 10.1186/s12891-017-1479-3.
31. Nuaez M., Nuaez E., Sastre S., Del-Val J.L. Prevalence of knee osteoarthritis and analysis of pain, rigidity, and functional incapacity. Orthopedics. 2008. 31(8). 753-754.
32. Oakley S.P., Lassere M.N. A critical appraisal of quantitative arthroscopy as an outcome measure in osteoarthritis of the knee. Arthritis Rheum. 2003. 33(2). 83-105. doi: 10.1016/s0049-0172(03)00082-9.
33. Paterson K.L., Sosdian L., Hinman R.S., Wrigley T.V., Kasza J., Dowsey M., Choong P., Bennell K.L. The influence of sex and obesity on gait biomechanics in people with severe knee osteoarthritis scheduled for arthroplasty. Clin. Biomech. (Bristol, Avon). 2017. 49. 72-77. doi: 10.1016/j.clinbiomech.2017.08.013.
34. Paterson K.L, Sosdian L., Hinman R.S., Wrigley T.V., Kasza J., Dowsey M., Choong P., Bennell K.L. Effects of sex and obesity on gait biomechanics before and six months after total knee arthroplasty: A longitudinal cohort study. Gait Posture. 2018. 61. 263-268. doi: 10.1016/j.gaitpost.2018.01.01.
35. Paterson K.L., Sosdian L., Hinman R.S., Wrigley T.V., Kasza J., Dowsey M., Choong P., Bennell K.L. The influence of sex and pre-operative obesity on biomechanics two years after total knee arthroplasty: A longitudinal cohort study. Gait Posture. 2020. 76. 74-84. doi: 10.1016/j.gaitpost.2019.10.031.
36. Phinyomark A., Osis S.T., Hettinga B.A., Kobsar D., Ferber R. Gender differences in gait kinematics for patients with knee osteoarthritis. BMC Musculoskelet. Disord. 2016. 17. 157. doi: 10.1186/s12891-016-1013-z.
37. Quintana J.M., Arostegui I., Escobar A., Azkarate J. Prevalence of knee and hip osteoarthritis and the appropriateness of joint replacement in an older population. Arch. Intern. Med. 2008. 168(14). 1576-1584.
38. Wang C., Huang S., Yu X., Jiang L., Bai Y., Lu Y., Wu X. Correlation Analysis on Early Gait and Prognosis Function after Total Knee Arthroplasty; Journal of Medical Biomechanics. 2018. 33(6). 558-563. DOI: 10.16156/j.1004-7220.2018.06.013.
39. Astephen Wilson J.L., Dunbar M.J., Hubley-Kozey C.L. Knee joint biomechanics and neuromuscular control du-ring gait before and after total knee arthroplasty are sex-specific. J. Arthroplasty. 2015. 30(1). 118-25. doi: 10.1016/j.arth.2014.07.028.
40. Xubo W., Lixi C, Lianbo X., Yong H, Shuyun J., Songbin Y., Yijie L. Research Article Early Spatiotemporal Patterns and Knee Kinematics during Level Walking in Individuals following Total Knee Arthroplasty. J. Health. Eng. 2017. 2017. 7056469. doi: 10.1155/2017/7056469. Epub 2017 Jul 31.