Международный эндокринологический журнал 5 (61) 2014
Вернуться к номеру
Профілактичний та лікувальний ефект воглібозу в менеджменті цукрового діабету
Авторы: Паньків В.І. - Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, м. Київ
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
У статті надано огляд ефектів інгібіторів альфа-глюкозидази — однієї з груп пероральних цукрознижувальних препаратів, які включені в Уніфікований клінічний протокол первинної і вторинної медичної допомоги при цукровому діабеті 2-го типу. Основна увага приділена воглібозу.
В статье приведен обзор эффектов ингибиторов альфа-глюкозидазы — одной из групп пероральных сахароснижающих препаратов, которые включены в Унифицированный клинический протокол первичной и вторичной медицинской помощи при сахарном диабете 2-го типа. Основное внимание уделено воглибозу.
The paper provided an overview of the effects of alpha-glucosidase inhibitors — one of the groups of oral hypoglycemic agents, which included in Standardized clinical protocol of primary and secondary health care in diabetes mellitus type 2. The main attention is paid to voglibose.
цукровий діабет, інгібітори альфа-глюкозидази, воглібоз.
сахарный диабет, ингибиторы альфа-глюкозидазы, воглибоз.
diabetes mellitus, alpha-glucosidase inhibitors, voglibose.
Статья опубликована на с. 83-87
На сьогодні в розпорядженні лікарів-клініцистів наявний досить широкий спектр лікарських препаратів для корекції гіперглікемії. Однак у країнах із середнім і низьким рівнем доходу на душу населення низка лікарських препаратів обмежено доступна. Крім того, для того, щоб фармакологічне лікування використовувалося ефективно і безпечно, безсумнівно, повинні розроблятися і впроваджуватися настанови до дії — алгоритми управління. Алгоритми — це інформація до клінічних роздумів, а саме: управління цукровим діабетом (ЦД) має бути індивідуальним, спрямованим на конкретного пацієнта. Розробка алгоритмів управління ЦД 2-го типу доволі складна з багатьох причин. Основною проблемою є обмежена доказова база стосовно вибору конкретних варіантів лікування або комбінацій препаратів, що можна проілюструвати таким прикладом. Якщо не враховувати модифікацію способу життя, станом на серпень 2014 року в нашому розпорядженні наявні цукрознижувальні препарати принаймні 7 терапевтичних класів: метформін, похідні сульфонілсечовини (ПСС), включно з глінідами, інгібітори альфа-глюкозидази, тіазолідиндіони, інгібітори дипептидилпептидази-4 (ДПП-4), агоністи рецепторів глюкагоноподібного пептиду-1 (ГПП-1) та інсулін. Якщо терапію розпочинають з одного з п’яти класів пероральних препаратів і адекватний контроль глікемії не досягається, вибирають другий препарат з шести класів. Якщо потрібен третій препарат, залишається ще 5 класів, з яких можна вибрати, і, нарешті, якщо призначають четвертий препарат, залишається ще 4 класи для вибору. Це означає, що існує 150 варіантів (5 • 6 • 5) потрійної терапії і 600 варіантів (5 • 6 • 5 • 4) терапії чотирма препаратами, і це без урахування поєднань препаратів у рамках одного класу, наприклад базального інсуліну і премікс–інсулінів. Отже, цілком очевидно, що алгоритми лікування не можуть бути по-справжньому науково обґрунтованими, зважаючи на відсутність порівняльних досліджень для всіх доступних комбінацій препаратів. Тому можна розробити засновані на доказах консенсусні алгоритми, хоча в таких випадках важливий баланс наявних доказів і консенсусу експертів, щоб уникнути потенційних помилок, що трапляються в деяких алгоритмах (Аметов А.С., 2014).
Інгібітори альфа-глюкозидази, як одна з груп пероральних цукрознижувальних препаратів, включені в Уніфікований клінічний протокол первинної і вторинної (спеціалізованої) медичної допомоги при цукровому діабеті 2-го типу, затверджений Міністерством охорони здоров’я України від 21.12.2012, Наказ № 1118. До групи інгібіторів альфа-глюкозидази належать засоби, які конкурентно інгібують ферменти шлунково-кишкового тракту, що беруть участь у розщепленні і всмоктуванні вуглеводів. У світі цей клас препаратів (А10BF) представлений акарбозою (А10BF01), міглітолом (А10BF02) і воглібозом (А10BF03).
Як відомо, постпрандіальна гіперглікемія сприяє розвитку серцево-судинних захворювань (ССЗ) та атеросклерозу, індукуючи оксидативний стрес, окиснення ліпопротеїнів низької щільності, активацію тромбоцитів та ендотеліальну дисфункцію у хворих на ЦД. Принцип дії інгібіторів альфа-глюкозидази, зокрема воглібозу, ґрунтується на конкурентному інгібуванні ферментів та зниженні швидкості вивільнення глюкози зі складних вуглеводів, що призводить до зменшення постпрандіальної гіперглікемії. Тому зменшення постпрандіальної гіперглікемії за допомогою воглібозу призводить до зниження рівня оксидативного стресу та маркерів запалення у хворих на ЦД (Satoh N. et al., 2006).
У дослідженні F. Santilli et al. (2010) було оцінено ефект інгібіторів альфа-глюкозидази на активацію тромбоцитів у пацієнтів з ЦД 2-го типу. Рандомізованим групам пацієнтів протягом 20 тижнів здійснювали терапію інгібіторами альфа-глюкозидази та плацебо. Після 8 тижнів у пацієнтів, які приймали інгібітори альфа-глюкозидази, спостерігалося зниження рівня 11-дегідро-тромбоксану-Б2 у сечі (маркера активації тромбоцитів in vivo) на 40 %, а також зниження екскреції 8-ізо-простагландину-F2а (8-ізо-ПГF2а) (маркера перекисного окиснення ліпідів in vivo) на 33 % відносно початкових показників порівняно з пацієнтами, які отримували плацебо. Лікування інгібітором альфа-глюкозидази сприяло зменшенню рівня постпрандіальної глюкози у плазмі (попередник 11-дегідро-тромбоксану-Б2) та середньої амплітуди коливання рівня глюкози (попередник 8-ізо-ПГF2а), що, у свою чергу, призвело до зниження оксидативного стресу та активації тромбоцитів.
В іншому дослідженні проведено оцінку здатності воглібозу знижувати маркери оксидативного стресу та рівні розчинних адгезивних молекул шляхом покращення постпрандіального стану у хворих на ЦД 2-го типу з ожирінням. 30 хворих були рандомізовано поділені на дві групи, одна з яких протягом трьох тижнів дотримувалася дієти (контрольна група), а друга поєднувала дієту з прийомом воглібозу (0,9 мг на день; група воглібозу). На початку дослідження в обох групах було відзначено підвищення рівня глюкози у плазмі після сніданку та обіду відносно показників до прийому їжі (p < 0,01). Унаслідок тритижневої терапії воглібозом рівень глюкози у плазмі до сніданку та після сніданку/обіду був значно нижчим (p < 0,01), у той час як у контрольній групі змін не спостерігалося (рис. 1) (Satoh N. et al., 2006).
У пацієнтів, які отримували воглібоз, встановлено зниження рівнів розчинних молекул міжклітинної адгезії 1 (sICAM-1), екскреції з сечею 8-ізо-ПГF2а, 8-гідрокси-2-дезоксигуанозину та вмісту С-реактивного білка (СРБ) у плазмі порівняно з показниками пацієнтів контрольної групи (табл. 1).
Отже, воглібоз довів свою здатність зменшувати частоту виникнення оксидативного стресу та рівень sICAM-1, а також знижувати постпрандіальну гіперглікемію у хворих на ЦД 2-го типу з ожирінням.
Одним з основних і найефективніших завдань боротьби з ЦД є зниження надмірної маси тіла. Відомо, що побічним ефектом певних груп цукрознижувальних препаратів (ПСС та ін.) є збільшення маси тіла. Воглібоз ефективно покращує глікемічний контроль та сприяє зменшенню глікованого гемоглобіну (HbA1c) в середньому на 2 % без побічного впливу на збільшення маси тіла.
K. Takami et al. (2002) провели дослідження з метою порівняльної оцінки впливу тільки дієти та дієти, поєднаної із застосуванням воглібозу або глібуриду, на абдомінальне ожиріння та метаболічні порушення у 36 пацієнтів з уперше діагностованим ЦД 2-го типу віком 50,8 ± 8,6 року, індекс маси тіла (ІМТ) — 24,5 ± 3,5 кг/м2. Протягом трьох місяців учасники дослідження дотримувалися дієти (n = 15; 30 ккал/кг на день), крім дієти приймали воглібоз (n = 12) або глібурид (n = 9).
Після лікування показники зменшення маси тіла були аналогічними в усіх трьох групах (група дієти — 2,7 ± 2,8 кг, група дієти та воглібозу — 2,6 ± 2,2 кг, група дієти та глібуриду — 3,1 ± 2,4 кг). Зменшення вісцеральної жирової тканини (ВЖТ) у групах було таким: 25,8 ± 20,7 % (група дієти), 30,7 ± 12,5 % (група дієти та воглібозу) та 30,2 ± 20,1 % (група дієти та глібуриду). Показники зменшення маси підшкірної жирової тканини (ПЖТ) дорівнювали 17,2 ± 24,0 % у групі дієти, 16,3 ± 19,6 % — у групі дієти та воглібозу, 19,3 ± 16,9 % — у групі дієти та глібуриду. Водночас співвідношення ВЖТ/ПЖТ було значно нижчим у групі дієти та воглібозу порівняно з аналогічним показником до терапії. Крім того, терапія воглібозом сприяла покращенню чутливості до інсуліну у хворих на ЦД 2-го типу.
Товщина комплексу інтима-медіа каротидної артерії (ТІМ) є одним із показників атеросклеротичної судинної патології. ТІМ каротидної артерії знаходиться у прямому взаємозв’язку з основними чинниками ризику ССЗ. Інгібітори альфа-глюкозидази довели свою ефективність відносно контролю приросту ТІМ каротидної артерії у хворих на ЦД. За даними метааналізу рандомізованих контрольованих досліджень, терапія інгібіторами альфа-глюкозидази сприяє значному зменшенню щорічного приросту ТІМ каротидної артерії, а також суттєвому уповільненню приросту ТІМ каротидної артерії в осіб з порушеною толерантністю до глюкози (ПТГ). Крім того, терапія інгібіторами альфа-глюкозидази вірогідно збільшує рівень холестерину ліпопротеїнів високої щільності (ЛПВЩ) та зменшує інсулінову резистентність, рівень HbA1c, тригліцеридів та діастолічного артеріального тиску (Geng D.F. et al., 2011).
Воглібоз як інгібітор альфа-глюкозидази зменшує рівні маркерів оксидативного стресу та приросту ТІМ каротидної артерії. Воглібоз запобігає подальшій абсорбції олігосахаридів у кишечнику та постпрандіальному збільшенню рівня глюкози в крові.
У відкритому рандомізованому проспективному дослідженні було встановлено ефективність тривалого застосування воглібозу щодо показників приросту ТІМ каротидної артерії у хворих на ЦД 2-го типу (Yamasaki Y. et al., 2005). Воглібоз у дозі 0,4–0,6 мг/добу було включено до схеми лікування 53 із 103 хворих на ЦД 2-го типу, які перебували на монотерапії дієтою, а також застосовували ПСС або інсулін. За учасниками дослідження спостерігали протягом трьох років для оцінки середньої та максимальної ТІМ каротидної артерії. У цей період вимірювалася ТІМ каротидної артерії з впливом воглібозу та без нього, разом з іншими клінічними показниками (HbA1c, ліпідний профіль, ІМТ та ін.).
За результатами дослідження, включення воглібозу до терапії запобігало збільшенню середньої та максимальної ТІМ каротидної артерії. Згідно з даними мультиваріантного регресивного аналізу, прийом воглібозу призводить до незалежного зменшення середньої ТІМ каротидної артерії на 0,069 мм/рік (p < 0,0001). Крім того, воглібоз значною мірою знижує рівень HbA1c, загального холестерину та тригліцеридів. Також він призводить до підвищення концентрації холестерину ЛПВЩ. У пацієнтів, які не отримували воглібоз, встановлено вірогідне збільшення середньої та максимальної ТІМ каротидної артерії. Отже, воглібоз призводить до зменшення ТІМ та може розглядатися і як антиатеросклеротичний препарат для хворих на ЦД 2-го типу.
Як відомо, акарбоза була першим доступним інгібітором альфа-глюкозидази в лікуванні ЦД. Головним недоліком акарбози є висока частота порушень функцій шлунково-кишкового тракту, включаючи метеоризм, здуття живота та діарею, що зменшує прихильність пацієнта до лікування (Kumar R.V., Sinha V.R., 2012) і змушує дати відповідь на питання стосовно безпеки цієї групи препаратів.
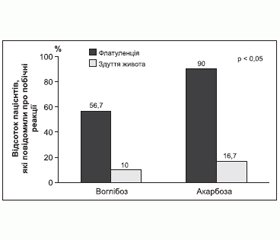
A. Vichayanrat et al. (2002) провів рандомізоване перехресне відкрите порівняльне дослідження з метою оцінки ефективності та безпеки воглібозу та акарбози при лікуванні ЦД 2-го типу у 30 пацієнтів на тлі дієтотерапії. Через 4 та 8 тижнів після початку лікування використання досліджуваних препаратів не показало вірогідного зменшення рівня глюкози натще. У той же час рівень постпрандіальної глікемії був вірогідно нижчим після терапії воглібозом та акарбозою через 4 та 8 тижнів. Зменшення показника постпрандіальної глікемії було пов’язане зі значним зниженням імунореактивного інсуліну та HbA1c у плазмі після 4 та 8 тижнів прийому воглібозу та акарбози.
У даному дослідженні побічні реакції з боку шлунково-кишкового тракту, зокрема метеоризм та здуття живота, у більшості випадків були спричинені застосуванням акарбози (p < 0,05; рис. 2).
/85/85.jpg)
Крім того, у дослідженні було встановлено вірогідне зниження маси тіла на 0,9 та 0,8 кг після 8 тижнів лікування воглібозом та акарбозою відповідно. За результатами дослідження, несприятливі побічні симптоми спостерігалися у 3,3 % пацієнтів, які отримували воглібоз, та у 43,4 % пацієнтів, які приймали акарбозу. Отже, воглібоз у дозі 0,2 мг призводив до розвитку меншої кількості побічних реакцій з боку шлунково–кишкового тракту.
Враховуючи гетерогенність ЦД 2-го типу, пов’язану з дисфункцією b-клітин, інсулінорезистентністю у периферичних тканинах та печінці, підвищеними рівнями вільних жирних кислот та прозапальних медіаторів, запізнілу діагностику, багатьом пацієнтам не вдається досягти належного глікемічного контролю. Як наслідок, все більше хворих на ЦД 2-го типу потребують терапії двома або більше цукрознижувальними препаратами для досягнення та підтримання цільового рівня глікемії. При цьому слід враховувати можливий вплив одного з комбінованих препаратів на підвищення моторики шлунково-кишкового тракту і порушення абсорбції інших препаратів.
У мультицентровому дослідженні N. Saito et al. (1998) оцінювали вплив воглібозу на глікемічний контроль у 86 хворих на ЦД 2-го типу. Протягом 24 тижнів дослідження пацієнтам було призначено пероральний прийом 0,6 мг воглібозу тричі на день до їжі, при цьому без припинення вживання звичного препарату сульфонілсечовини. У цих пацієнтів установлено вірогідне зниження рівнів глікемії натще, постпрандіальної глікемії та HbA1c відносно початкових показників (p < 0,05) практично на всіх етапах лікування. Істотного впливу терапії на зміну маси тіла пацієнтів не відзначено. У 65 % хворих покращився контроль глюкози у крові, у 92,9 % пацієнтів терапія не спричинила жодних побічних реакцій. Дослідження довело, що комбінування воглібозу та препаратів сульфонілсечовини є ефективним у хворих на ЦД 2-го типу.
В іншому дослідженні було встановлено здатність воглібозу впливати на фармакокінетику глібенкламіду та рівень глюкози плазми натще після прийому глібенкламіду. У подвійне сліпе перехресне дослідження було включено 12 здорових чоловіків, які отримали одноразову дозу 1,75 мг глібенкламіду на восьмий день тривалого застосування плацебо (порівняння) або 5 мг воглібозу тричі на день (контроль). За результатами дослідження, співвідношення «концентрація — час» для глібенкламіду у випадку його поєднаного застосування з воглібозом було аналогічним для плацебо. Крім того, зниження рівня глюкози плазми натще після прийому глібенкламіду залишилося незмінним після включення плацебо або воглібозу до схеми терапії. Це доводить, що воглібоз не взаємодіє з глібенкламідом на фармакокінетичному рівні. Також дослідження дозволяє зробити висновок щодо доброї переносимості та безпеки клінічного застосування воглібозу та глібенкламіду (Kleist P. et al., 1997).
Ще в одному дослідженні спостерігали за ефективністю інгібітора альфа-глюкозидази у 36 пацієнтів з ЦД 2-го типу (середня тривалість захворювання 8,8 ± 0,9 року). Усі хворі на тлі дієти приймали або препарат сульфонілсечовини, або комбінацію сульфонілсечовини з метформіном. Ці пацієнти протягом шести місяців додатково отримували інгібітор альфа-глюкозидази. За результатами дослідження, включення інгібітору альфа-глюкозидази до схеми лікування «дієта + ПСС» або «дієта + ПСС + метформін» призводить до суттєвого покращення глікемічного контролю (Vannasaeng S. et al., 1995).
M. Abe et al. (2007) провели відкрите рандомізоване дослідження за участі 31 хворого на ЦД на гемодіалізі з нестабільним глікемічним контролем. Хворі були рандомізовано поділені на групи комбінованої терапії піоглітазоном (фіксована доза 30 мг) і воглібозом та монотерапії воглібозом (контрольна група). Згідно з результатами цього дослідження, 30 мг піоглітазону на день є ефективними у пацієнтів на гемодіалізі з ожирінням та без нього. Комбінація піоглітазону та воглібозу сприяє досягненню належного глікемічного контролю у таких хворих на ЦД 2-го типу.
Хотілося б підкреслити також можливість використання воглібозу для профілактики виникнення ЦД 2-го типу в осіб з ПТГ. Японські дослідники (Kawamori R. et al., 2009) вивчали ефективність воглібозу з метою профілактики ЦД 2-го типу в 1780 осіб із ПТГ в багатоцентровому рандомізованому подвійному сліпому дослідженні.
Учасники дослідження були розділені на групи прийому воглібозу (n = 897) в дозі 0,2 мг тричі на день або плацебо (n = 883). Лікування тривало аж до розвитку ЦД 2-го типу (первинна кінцева точка), або досягнення нормоглікемії (вторинна кінцева точка), або принаймні 3 роки.
Встановлено, що особи з ПТГ, які отримували воглібоз, мали низький ризик її прогресування до ЦД 2-го типу порівняно з плацебо. Набагато більше людей з групи воглібозу досягнули стану нормоглікемії, ніж з групи плацебо (599 з 897 проти 454 з 881; p < 0,0001). 810 (90 %) з 897 осіб з групи воглібозу відзначали побічні ефекти порівняно з 750 (85 %) з 881 в групі плацебо. Автори дійшли висновку, що призначення воглібозу на додаток до модифікації способу життя дає змогу зменшити ризик розвитку ЦД 2-го типу в осіб із ПТГ.
Слід підкреслити, що побічні ефекти з боку шлунково-кишкового тракту є фізіологічними (метеоризм і здуття живота) і зникають через 2–3 місяці прийому інгібіторів альфа-глюкозидази. Зазвичай вони спостерігаються при порушенні режиму харчування (надмірному споживанні вуглеводів). Тому можна вважати, що воглібоз є своєрідним засобом контролю для пацієнта з ЦД. Наявність метеоризму — це ніби лакмусовий папірець, що вказує на погрішності в дієті. При дотриманні дієтичного режиму побічні явища не розвиваються.
Інгібітори альфа-глюкозидази широко використовуються і популярні у багатьох країнах, особливо азіатських. Hanefeld et al. провели метааналіз впливу інгібіторів альфа-глюкозидази на частоту серцево-судинних подій в 7 рандомізованих плацебо-контрольованих дослідженнях з тривалістю спостереження не менше 52 тижнів і виявили вірогідне зниження ризику розвитку інфаркту міокарда і будь-якої серцево-судинної події.
В Україні нещодавно зареєстрований препарат воглібозу — Воксид (виробництво ТОВ «Кусум Фарм», Україна). Препарат випускається в таблетках по 0,2 або 0,3 мг для вживання всередину безпосередньо перед їжею. Показаннями до призначення препарату Воксид є ЦД 2-го типу, якщо рівень глюкози в крові неможливо адекватно підтримувати тільки дієтою або фізичними вправами. Воксид призначається як монотерапія або у складі комбінованої терапії з іншими цукрознижувальними засобами або з інсуліном. Крім того, Воксид можна призначати і при лікуванні ЦД 1-го типу разом з препаратами інсуліну. Дуже важливим показанням є профілактика ЦД 2-го типу в осіб із вперше виявленим порушенням толерантності до глюкози.
1. Abe M., Kikuchi F., Kaizu K. et al. Combination therapy of pioglitazone with voglibose improves glycemic control safely and rapidly in Japanese type 2-diabetic patients on hemodialysis // Clin. Nephrol. — 2007. — Vol. 68(5). — P. 287–294.
2. Geng D.F., Jin D.M., Wu W. et al. Effect of alpha-glucosidase inhibitors on the progression of carotid intima-media thickness: a meta-analysis of randomized controlled trials // Atherosclerosis. — 2011. — Vol. 218(1). — P. 214–219.
3. Kumar R.V., Sinha V.R. Newer insights into the drug delivery approaches of glucosidase inhibitors // Expert. Opin. Drug. Deliv. — 2012. — Vol. 9(4). — P. 403–416.
4. Saito N., Sakai H., Suzuki S. et al. Effect of an alpha-glucosidase inhibitor (voglibose), in combination with sulphonylureas, on glycaemic control in type 2 diabetes patients // J. Int. Med. Res. — 1998. — Vol. 26(5). — P. 219–232.
5. Santilli F., Formoso G., Sbraccia P. et al. Postprandial hyperglycemia is a determinant of platelet activation in early type 2 diabetes mellitus // J. Thromb. Haemost. — 2010. — Vol. 8(4). — P. 828–837.
6. Satoh N., Shimatsu A., Yamada K. et al. An alpha-glucosidase inhibitor, voglibose, reduces oxidative stress markers and soluble intercellular adhesion molecule 1 in obese type 2 diabetic patients // Metabolism. — 2006. — Vol. 55(6). — P. 786–793.
7. Takami K., Takeda N., Nakashima K. et al. Effects of die-tary treatment alone or diet with voglibose or glyburide on abdominal adipose tissue and metabolic abnormalities in patients with newly diagnosed type 2 diabetes // Diabetes Care. — 2002. — Vol. 25(4). — P. 658–662.
8. Vannasaeng S., Ploybutr S., Nitiyanant W. et al. Effects of alpha-glucosidase inhibitor (acarbose) combined with sulfonylurea or sulfonylurea and metformin in treatment of non-insulin-dependent diabetes mellitus // J. Med. Assoc. Thai. — 1995. — Vol. 78(11). — P. 578–585.
9. Vichayanrat A., Ploybutr S., Tunlakit M. et al. Efficacy and safety of voglibose in comparison with acarbose in type 2 diabetic patients // Diabetes Res. Clin. Pract. — 2002. — Vol. 55(2). — P. 99–103.
10. Yamasaki Y., Katakami N., Hayaishi-Okano R. et al. Alpha-Glucosidase inhibitor reduces the progression of carotid intima-media thickness // Diabetes Res. Clin. Pract. — 2005. — Vol. 67(3). — P. 204–210.

/84/84.jpg)
/84/84_2.jpg)