Международный эндокринологический журнал 6 (62) 2014
Вернуться к номеру
Интеллект ребенка и йодный дефицит: механизмы негативного влияния и пути профилактики
Авторы: Бережной В.В., Маменко М.Е. - Национальная медицинская академия последипломного образования им. П.Л. Шупика МЗ Украины, г. Киев
Рубрики: Педиатрия/Неонатология, Эндокринология
Разделы: Справочник специалиста
Версия для печати
В статье приведен обзор научной литературы о влиянии йодного дефицита на интеллектуальное развитие ребенка. Сделан вывод о необходимости применения массовой йодной профилактики в популяции и индивидуальной — в группах повышенного риска развития йододефицитных заболеваний, к которым относятся дети, беременные, кормящие матери.
У статті наведено огляд наукової літератури щодо впливу йодного дефіциту на інтелектуальний розвиток дитини. Зроблено висновок про необхідність застосування масової йодної профілактики у популяції та індивідуальної — в групах підвищеного ризику розвитку йододефіцитних захворювань, до яких відносяться вагітні, матері-годувальниці та діти грудного віку.
The paper presents a review of scientific literature on the effect of iodine deficiency on the intellectual development of the child. The conclusion was made about the need for a mass iodine prophylaxis in the population and the individual one — in groups at high risk of iodine deficiency disorders, which include children, pregnant women and nursing mothers.
йодный дефицит, беременность, кормящая мать, дети, йодная профилактика.
йодний дефіцит, вагітність, мати-годувальниця, діти, йодна профілактика.
iodine deficiency, pregnancy, nursing mother, children, iodine prophylaxis.
Статья опубликована на с. 41-45
Влияние йодного дефицита (ЙД) на интеллектуальные способности человека выступает в качестве одного из основных аргументов сторонников внедрения массовой и индивидуальной йодной профилактики в странах, где ЙД является проблемой национального уровня. На негативное влияние недостатка йода как эссенциального микроэлемента в продуктах питания на развитие мозга делает акцент Детский фонд ООН (ЮНИСЕФ), разрабатывая программы информационной работы с населением. Однако именно связь йодного дефицита с ментальными способностями человека остается наиболее дискутабельной в научной среде с учетом многофакторности влияния на интеллект (наследственность, среда, воспитание, питание и т.д.).
Безусловно, йод как микроэлемент не участвует в формировании мозговых структур, ответственных за осуществление мыслительных процессов. Однако роль йодсодержащих гормонов щитовидной железы (ЩЖ) в формировании и регуляции функциональной активности центральной нервной системы (ЦНС) неоспорима.
В энциклопедии Дени Дидро, изданной в 1754 году во Франции, дано следующее определение термина «кретин»: «ненормальный глухой человек с зобом, который свисает до талии». Наполеон Бонапарт, который с помощью своего войска мечтал покорить всю Европу, первым заметил, что большинство солдат, призванных на военную службу из горных районов, страдают тугоухостью, отстают в физическом и умственном развитии, быстро утомляются, что делает их практически непригодными к участию в военных походах.
Йод и щитовидная железа
Адекватное поступление йода является ключевым требованием для осуществления тиреоидного синтеза. Йод из продуктов питания в пищеварительном тракте трансформируется в йодид калия и с током крови транспортируется в ЩЖ при помощи натрий/йод симпортера. На апикальной мембране тиреоцита при помощи фермента тиреопероксидазы (ТПО) и перекиси водорода происходит окисление йода и его присоединение к тирозольному остатку тиреоглобулина с образованием монойодтирозина и дийодтирозина. Эти два соединения являются прекурсорами тиреоидных гормонов (ТГ). Под влиянием ТПО соединение монойодтирозина и дийодтирозина приводит к образованию трийодтироксина (Т3), а слияние двух дийодтирозинов формирует тироксин (Т4). Йод соcтавляет 59 % молекулярной массы трийодтиронина и 65 % — тироксина. Щитовидная железа синтезирует в 4–5 раз больше Т4, чем Т3. Трийодтиронин образуется путем монодейодинации тироксина преимущественно на периферии [1, 9, 11].
Действие тиреоидных гормонов
Основные эффекты тиреоидных гормонов опосредуются через нуклеарные рецепторы к ТГ. По сути, последние играют роль факторов транскрипции ДНК (табл. 1). Концентрация в сыворотке крови Т4 превышает Т3 в 80–100 раз. При этом свою активность тироксин реализует преимущественно путем конвертации в трийодтиронин, имеющий в 10 раз более высокое сродство к нуклеарным рецепторам [9, 11].
Йодный дефицит и йододефицитные заболевания
Многочисленные негативные явления, возникающие вследствие ЙД (табл. 2), обусловливаются неадекватным синтезом тиреоидных гормонов (ТГ) [13, 14]. Причем нарушения ментальных функций разной степени выраженности могут наблюдаться в любом возрасте, однако поддержка тиреоидного гомеостаза является наиболее критичной в течение антенатального периода и первых двух-трех лет жизни [7, 8].
В развитии ЦНС ребенка, с точки зрения влияния тиреоидных гормонов, выделяют 3 периода: I — до 10–12 недель беременности; II — с 12-й недели беременности до родов; ІІІ — постнатальный период [1, 5].
В первом периоде плод полностью зависим от материнских тиреоидных гормонов. На этапе внутриутробного развития именно ТГ матери являются важнейшими регуляторами формирования и развития головного мозга плода. В это время происходит нейрогенез и существует высокий риск поражения головного мозга вследствие гипотироксинемии беременной. На ранних этапах внутриутробного развития, когда закладываются основные церебральные структуры, именно ТГ регулируют экспрессию ряда генов, обеспечивающих развитие ЦНС плода, и синтез специфических белков. Одним из таких белков является нейрогранин, функционирующий как «третий мессенджер» в каскаде протеинкиназы С, которая обеспечивает синаптическое ремоделирование в нейронах. При дефиците ТГ содержание нейрогранина в головном мозге уменьшается, в результате чего на любом этапе формирования мозга могут произойти необратимые изменения, проявляющиеся в дальнейшем нарушением интеллектуального и моторного развития ребенка различной степени тяжести. Даже незначительное и/или транзиторное снижение уровня свободного тироксина во время беременности угрожает формированием нарушений психомоторного развития ребенка в последующем [8, 10].
В течение первых трех месяцев беременности материнские ТГ обеспечивают формирование наиболее значимых структур головного мозга плода (коры, подкорковых ядер, мозолистого тела, субарахноидальных путей), улитки слухового анализатора, глаз, лицевого скелета, легочной ткани и др. В случае дефицита ТГ матери в этот период ребенок имеет характерные расстройства, которые зависят от степени йодного дефицита и проявляются различными нарушениями: от эндемического кретинизма до легких психомоторных нарушений, проявляющихся расстройствами моторики и речи, неуклюжестью. Изменения, произошедшие на этапе дифференцировки головного мозга, являются фатальными и в последующем не поддаются коррекции [8, 12, 13].
/44/44.jpg)
После 12-й недели беременности (во втором периоде) имеет место сочетанное влияние материнских и фетальных ТГ, которые регулируют процессы созревания нейронов, нейрональную миграцию и симпатогенез. В это время в ткани головного мозга плода возрастает количество Т3-рецепторов. Со второй половины беременности, когда ЩЖ плода начинает активно функционировать, под влиянием собственных ТГ происходят процессы симпатогенеза и миелинизации нервных волокон, формируются ассоциативные связи и проводниковая система ЦНС, что в дальнейшем определяет способности ребенка к абстрактному мышлению. Снижение функциональной активности ЩЖ матери на этом этапе приводит к значительному ухудшению интеллектуальных способностей ребенка, однако своевременное выявление и коррекция нарушений в течение первого года жизни могут нормализовать процессы психомоторного развития [8, 12, 13].
На постнатальном этапе (третий период) уровень обеспеченности ребенка ТГ зависит исключительно от активности его собственной щитовидной железы, под контролем гормонов которой продолжаются процессы созревания нейронов, глиогенез, миелинизация. При этом мозг ребенка остается чрезвычайно чувствительным к дефициту ТГ в течение двух-трех лет жизни, а по некоторым источникам — и значительно дольше [2, 12].
Повышая уровень обменных процессов, усиливая энергетический обмен и обеспечивая прессорный катехоламиновый эффект, тиреоидные гормоны активизируют функциональную активность ЦНС, интеллектуальную работоспособность, способность к обучению на всех этапах жизни человека. Поэтому снижение уровня продукции ТГ всегда негативно влияет на интеллектуальные способности ребенка [10].
Доказано, что снижение интеллектуального коэффициента (IQ) населения в йододефицитных регионах обусловлено не ростом частоты случаев неврологического кретинизма, а увеличением количества людей с легкими ментальными и психомоторными нарушениями [2, 13]. Ментальные нарушения у детей часто становятся заметными только в школьном возрасте, что снижает возможность получения в будущем «интеллектуальных» профессий. Многочисленными исследованиями доказано, что в большинстве йододефицитных регионов интеллектуальный потенциал населения является уменьшенным на 10–15 % и зависит от степени йодной недостаточности. Более 2/3 детей, проживающих на таких территориях, имеют отклонения по тем или иным показателям интеллектуального развития, плохо учатся в школе, неудовлетворительно выполняют психомоторные тесты, имеют нарушения моторики, слуха и речи [13, 14].
Причиной ментальных нарушений в любом возрасте может быть скрытый или манифестный гипотиреоз [6, 7, 9]. Йодный дефицит является его наиболее распространенной причиной в странах с недостаточным йодным обеспечением населения, к которым относится вся территория Украины. Истинная распространенность данного патологического состояния значительно превышает данные официальной статистики в силу вариабельности и низкой специфичности клинических проявлений.
Как известно, гипотиреоз — клинический синдром, вызванный длительным и стойким недостатком гормонов щитовидной железы в организме или снижением их биологического эффекта на тканевом уровне. В основе клинических симптомов гипотиреоза лежит замедление процессов обмена веществ и энергии из-за недостаточного поступления ТГ в клетку. Среди клинических проявлений гипотиреоза наряду с повышенной чувствительностью к холоду, зябкостью, быстрой утомляемостью, сухостью кожных покровов, запорами часто наблюдается снижение памяти, замедление скорости восприятия. Способность к обучению у детей с гипотиреозом обычно выраженно не страдает, но замедляется темп мыслительных процессов и скорость выполнения работы. Распространенной клинической маской гипотиреоза является депрессия.
Наиболее распространенной формой приобретенного гипотиреоза, ассоциированного с йодным дефицитом у детей, является субклинический гипотиреоз.
Врожденный гипотиреоз (ВГ) — самая частая причина корригируемой задержки умственного развития. Наиболее распространенным в мире этиологическим фактором ВГ является дефицит йода. В странах с выраженным ЙД до 10 % новорожденных имеют риск развития гипотиреоза и его неврологических последствий [9, 11].
Эндемические формы гипотиреоза, развивающиеся вследствие тяжелого йодного дефицита, обозначаются как кретинизм. Выделены два основных вида кретинизма — неврологический и микседематозный.
Неврологический кретинизм часто встречается в Южной Америке и Южно-Тихоокеанском регионе. В неврологической симптоматике преобладают выраженная степень умственной недостаточности, глухонемота, спастическая диплегия и задержка роста.
Микседематозный кретинизм превалирует в эндемических регионах Африки и манифестирует преимущественно микседематозными симптомами, такими как крупные черты лица, сухая кожа, хриплый низкий голос, запор и карликовость.
Смешанная форма с симптомами как неврологического, так и микседематозного кретинизма также встречается в некоторых регионах, например в Гималаях.
При менее тяжелом йодном дефиците наблюдается разной степени выраженности снижение интеллекта, способности к обучению, тугоухость, зоб.
Таким образом, снижение функциональной активности щитовидной железы неизбежно оказывает негативное влияние на нервно–психическое развитие и формирование интеллекта ребенка. Для обеспечения адекватного тиреоидного гормоногенеза необходимым условием является достаточное ежедневное поступление данного микроэлемента в организм. Единственными продуктами питания, обеспечивающими достаточное поступление йода в организм, являются морепродукты. Население территорий, удаленных от морского побережья, нуждается в проведении постоянной йодной профилактики.
Методы профилактики нарушений ментальных функций вследствие йодного дефицита
Как известно, существует три основных вида йодной профилактики: массовая, индивидуальная и групповая [3, 4]. Все они базируются на дополнительном введении йода в организм человека, проживающего в йододефицитном регионе.
Массовая йодная профилактика. Поскольку проблема йодного дефицита носит глобальный характер, в мире наиболее эффективной признана массовая («немая») профилактика. Она состоит в том, что все население страны постоянно использует йодированную соль в качестве универсального носителя йода. Главным преимуществом такого подхода является поступление йода в профилактической дозе в организм каждого жителя страны независимо от его интеллектуального, образовательного и материального уровня. Именно всеобщее обязательное йодирование соли, которая используется в питании людей, является главным методом ликвидации йодного дефицита, рекомендованным ВОЗ, МСКЙДЗ и ЮНИСЕФ. Международный опыт свидетельствует о том, что для проведения массовой профилактики необходима всеобщая йодизация соли в стране, что требует принятия соответствующих законодательных актов. Спорадическое использование соли в отдельных домохозяйствах не дает желаемого профилактического эффекта в масштабах популяции. Кроме того, существуют специфические категории населения (беременные, кормящие женщины, дети грудного возраста, подростки), у которых решить проблему профилактики ЙД только с помощью употребления йодированной соли невозможно. Учитывая повышенную потребность в йоде у беременных и кормящих, дополнительная индивидуальная профилактика этим категориям населения осуществляется даже в странах, где налажена массовая система профилактики [3, 12–14].
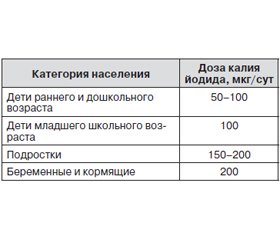
Групповая и индивидуальная профилактика. Для групповой и индивидуальной профилактики ныне действующими в Украине протоколами оказания помощи детям с заболеваниями щитовидной железы рекомендуются исключительно фармакологические препараты калия йодида [4].
Для предотвращения когнитивных нарушений у детей постоянная фармакологическая дотация йода беременным и кормящим женщинам является стратегически необходимой. Для них суточная потребность в йоде составляет 250 мкг/сут, и ее невозможно покрыть употреблением йодированной соли. В настоящее время эксперты международных организаций рекомендуют повысить дозу йода, поступающего в организм, еще на этапах планирования беременности (за 2–3 месяца до ее наступления). Кроме того, женщина должна получать дотацию 200 мкг йода ежедневно в течение всей беременности и лактации.
При искусственном вскармливании следует отдавать предпочтение смесям с содержанием йода для доношенных детей до 100 мкг/л, а для недоношенных — до 200 мкг/л готовой смеси. Во втором полугодии жизни в питание ребенка необходимо добавлять препарат калия йодида, который может быть растворен в любом получаемом блюде прикорма.
Недопустимо проводить йодную профилактику, используя всевозможные биологически активные добавки, которые не имеют четко определенного и, главное, контролируемого содержания йода в своем составе. При их употреблении человек может получить как недостаточное, так и избыточное количество йода, что в любом случае является нефизиологичным и небезопасным.
Выводы
Йодный дефицит — проблема, актуальная для всей территории Украины. Разнится только степень его тяжести — от легкого на востоке, юге и в центре страны до среднетяжелого и тяжелого в горных районах Крыма и Карпат. В условиях отсутствия массовой йодной профилактики имеет место высокая частота йододефицитных заболеваний у населения, в том числе нарушений ментальных функций различной степени выраженности.
Решить проблему профилактики ЙДЗ у населения можно, приняв на законодательном уровне решение об обязательном йодировании пищевой соли в стране, а также путем индивидуальной профилактики препаратами калия йодида в группах особого риска (дети и подростки, беременные и кормящие женщины). Профилактические меры должны быть постоянными, поскольку йодный дефицит как экологическую проблему ликвидировать невозможно. Мировой и отечественный опыт показывает, что прекращение профилактики приводит к быстрому росту частоты ЙДЗ в популяции.
1. Балаболкин М.И. Фундаментальная и клиническая тиреодология: Учеб. пособ. / Балаболкин М.И., Клебанова Е.М., Креминская В.М. — М.: Медицина, 2007. — 816 с.
2. Бєлих Н.А. Вплив гіпофізарно-тиреоїдної дезадаптації плода на розвиток та стан здоров’я дітей грудного віку / Н.А. Бєлих, М.Є. Маменко, О.І. Єрохіна // Современная педиатрия. — 2011. — № 1 (35). — С. 142–144.
3. Маменко М.Е. Профилактика йодного дефицита (к вопросу о необходимости принятия национальной программы) / М.Е. Маменко // Современная педиатрия. — 2010. — № 2. — С. 39–45.
4. Протокол з надання медичної допомоги дітям за спеціальністю «Дитяча ендокринологія»: наказ МОЗ України № 254 від 27.04.2006 р. / МОЗ України. — Київ, 2006. — 88 с. (Нормативний документ МОЗ України).
5. Сапронов Н.С. Нейрофизиологические эффекты тиреоидных гормонов / Н.С. Сапронов, О.О. Масалов // Психофармакология и биологическая наркология. — 2007. — Т. 7, № 2. — С. 1533–1541.
6. Фадеев В.В. Гипотиреоз / Фадеев В.В., Мельниченко Г.А. — М.: РКИ «Северопресс», 2005. — 286 с.
7. Behrooz H.G. Subclinical hypothyroidism in pregnancy: intellectual development of offspring / H.G. Behrooz, M. Tohidi, Ya. Mehrabi [et al.] // Thyroid. — 2011. — Vol. 21 (10). — P.1143–1147.
8. De Escobar G.M. Role of thyroid hormone during early brain development / G.M. de Escobar, M.J. Obregon, F. Escobar del Rey // European Journal of Endocrinology. — 2004. — Vol. 151. — P. 25–37.
9. Practical Paediatric Endocrinology in a Limited Resource Setting / Editor Zacharin M. — Melburne, Australia, 2011. — 320 p.
10. Raymond J. Fetal and neonatal thyroid function: review and summary of significant new findings / J. Raymond, S.H. La Franchi // Curr. Opin. Endocrinol. Diabetes Obes. — 2010. — № 17 (1). — Р. 1–7.
11. Raine Joseph E. Practical Endocrinology and Diabetes in Children / Raine Joseph E., Malcolm D.C. Donaldson, John W. Gregory, Guy Van Vilet. — 3rd edition. — Wiley–Blackwell. — 2010. — 258 p.
12. Zimmermann M.B. Iodine Deficiency // Endocrine Reviews. — 2009. — 30 (4). — P. 376–408.
13. Zimmermann M.B. Iodine-deficiency disorders / M.B. Zimmermann, P.L. Jooste, C.S. Pandav // Lancet. — 2008. — Vol. 372 (9645). — P. 1251–1262.
14. WHO, UNICEF, and ICCIDD. Assessment of the Iodine Deficiency Disorders and monitoring their elimination. Third edition. — Geneva: WHO, WHO/Euro/NUT. — 2007. — P. 1–98.

/42/42.jpg)