Международный эндокринологический журнал 1 (65) 2015
Вернуться к номеру
Показники центральної гемодинаміки у хворих на цукровий діабет 2-го типу з неалкогольною жировою хворобою печінки. Взаємозв’язок з фактором некрозу пухлини α та інтерлейкіном-6
Авторы: Черняєва А.О., Кравчун Н.О. — Державна установа «Інститут проблем ендокринної патології ім. В.Я. Данилевського НАМН України», м. Харків
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
У роботі вивчені показники центральної гемодинаміки у пацієнтів із цукровим діабетом 2-го типу в поєднанні з неалкогольною жировою хворобою печінки. Виявлено клінічно значуще підвищення показників запалення низької інтенсивності (фактор некрозу пухлини α, інтерлейкін-6), а також встановлено їх негативний кореляційний зв’язок із структурно-функціональними показниками лівого шлуночка, що свідчить про негативну роль фактора некрозу пухлини α та інтерлейкіну-6 в ремоделюванні міокарда.
В работе изучены показатели центральной гемодинамики у пациентов с сахарным диабетом 2-го типа в сочетании с неалкогольной жировой болезнью печени. Выявлено клинически значимое повышение показателей воспаления низкой интенсивности (фактор некроза опухоли α, интерлейкин-6), а также установлена их отрицательная корреляционная связь со структурно-функциональными показателями левого желудочка, что свидетельствует о негативной роли фактора некроза опухоли α и интерлейкина-6 в ремоделировании миокарда.
We studied central hemodynamics in patients with type 2 diabetes mellitus combined with non-alcoholic fatty liver disease. There were determined a clinically significant aggravation inflammation processes of low intensity (tumor necrosis factor α, interleukin 6), as well as their negative correlation with the structural and functional parameters of left ventricle, indicating a negative role of tumor necrosis factor α and interleukin 6 in myocardial remodeling.
цукровий діабет 2-го типу, неалкогольна жирова хвороба печінки, кардіогемодинаміка, фактор некрозу пухлини α, інтерлейкін-6.
сахарный диабет 2-го типа, неалкогольная жировая болезнь печени, кардиогемодинамика, фактор некроза опухоли α, интерлейкин-6.
type 2 diabetes mellitus, non-alcoholic fatty liver disease, cardiac hemodynamics, tumor necrosis factor α, interleukin 6.
Статья опубликована на с. 53-56
Вступ
Останніми десятиріччями цукровий діабет (ЦД) — найбільш поширене захворювання у сучасному світі, головним чином за рахунок ЦД 2-го типу. ЦД пов’язаний з медичними та соціально-економічними причинами, що не дає підстави для оптимістичних прогнозів [1, 2]. Серцево-судинні захворювання (ССЗ) — найчастіші ускладнення та провідна причина смертності та інвалідизації пацієнтів з ЦД 2-го типу [3, 4]. Незважаючи на той факт, що первинні чинники, що викликають ЦД 2-го типу, до кінця невідомі, інсулінорезистентність (ІР) вважається ключовою ознакою захворювання [5, 6] та є важливою складовою в патофізіології низки хронічних захворювань, включаючи артеріальну гіпертензію (АГ), ішемічну хворобу серця (ІХС) та метаболічний синдром [7]. У свою чергу, ІР призводить до розвитку стеатозу печінки через порушення здатності інсуліну пригнічувати ліполіз (переважно у вісцеральних адипоцитах) і таким чином збільшує надходження вільних жирних кислот (ВЖК) до печінки. Надлишок постачання ВЖК, у свою чергу, сприяє розвитку та прогресуванню ІР в печінці [8] та запуску патологічної дії прозапальних цитокінів. Натепер вважають, що хронічне запалення низької інтенсивності відіграє важливу роль в патогенезі як ІР, так і ЦД 2-го типу [9]. Отримані дані, що прозапальний цитокін — фактор некрозу пухлини альфа (ФНП-альфа) може вважатися маркером ССЗ та кардіоваскулярного ризику, оскільки рівень даного цитокіну підвищується у хворих на АГ та більшою мірою — у хворих з підвищеною масою тіла та абдомінальним типом ожиріння [9–12]. Жирова тканина при ожирінні залучена до запалення та секретує велику кількість прозапальних цитокінів, таких як ФНП-альфа, інтерлейкіни (ІЛ), зокрема ІЛ-6. Незважаючи на те, що рівні ФНП-альфа та ІЛ-6 підвищені при ожирінні, вони є низькими порівняно з такими в тканині [10, 13].
На вiдмiну вiд ФНП-альфа IЛ-6 проявляє свою активність не лише в жировiй тканинi, але й системно [14, 15]. Доведено, що рівень експресії гена IЛ-6 у жировій тканинi позитивно корелює як зi ступенем активування утилiзацiї глюкози, так i з вираженістю ІР.
Натепер є поодинокі дослідження щодо внеску ФНП-альфа та ІЛ-6 в розвиток серцево-судинних ускладнень у хворих на ЦД 2-го типу. Викликає інтерес визначення вказаних цитокінів у хворих на ЦД 2-го типу з неалкогольною жировою хворобою печінки (НАЖХП).
Мета дослідження — вивчення взаємозв’язків показників кардіогемодинаміки з активністю ФНП-а та ІЛ-6 у хворих на ЦД 2-го типу з НАЖХП.
Матеріали та методи
Обстежено 106 хворих (62 жінки та 44 чоловіки) віком від 51 до 79 років (середній вік — 69,88 ± 1,14 року), які страждають від ЦД 2-го типу в поєднанні з НАЖХП (глікемія натще < 7,6 ммоль/л, постпрандіальна < 9,0 ммоль/л, глікований гемоглобін (НbA1c) < 8,5 %). Тривалість ЦД 2-го типу — від 1 до 10 років (середня — 9,7 ± 0,9 року).
Мікросудинні ускладнення спостерігалися у 50 % обстежених, ІХС діагностовано у всіх хворих, а в поєднанні з гіпертонічною хворобою (ГХ) — у 70 %.
В обстежених хворих визначали клінічні дані та загальний холестерин (ЗХС) [16], бета-ліпопротеїди [17], тригліцериди [18], С-пептид (норма — 0,5–3,2 нг/мл), НbA1c (норма — 4–5,9 %) [19]. Цукор крові натще та цукор крові постпрандіальний визначали глюкозооксидазним методом за допомогою апарата «Ексан» [20], уміст у плазмі крові фібриногену — ваговим методом [21], фібрину — спектрофотометричним методом [22] (нормальні показники фібриногену — 2–4 г/л, фібрину — 9–18 мг).
ІЛ-6 (норма — 50–80 нг/мл) вимірювали у сироватці крові імуноферментним методом із використанням набору реагентів А-8768 виробництва «Вектор-Бест», Росія.
ФНП-альфа (норма — 55,8–90,1 пг/мл) визначали за допомогою набору «Альфа-ФНО-ИФА-Бест» виробництва «Вектор-Бест», Росія.
Ехокардіографічне (ЕхоКГ) дослідження проводили в одно- та двовимірному режимах за допомогою апарата RADMIR (UltimaPRO 30) (Харків, Україна). Сканування здійснювали датчиком із частотою 3,5 МГц з парастернальної та апікальної позицій. Визначали наступні показники: кінцево-діастолічний розмір (КДР), кінцево-систолічний розмір (КСР), товщину стінки міжшлуночкової перегородки (ТСМШП), масу міокарда лівого шлуночка та індекс маси міокарда лівого шлуночка (ІММЛШ) [23]. Оцінку систолічної функції лівого шлуночка проводили згідно з наступними показниками: кінцево-діастолічним об’ємом (КДО), кінцево-систолічним об’ємом (КСО), ударним об’ємом (УО), хвилинним об’ємом (ХО), фракцією викиду (ФВ), товщиною стінки міокарда лівого шлуночка або 2Н/D, розміром аорти та лівого передсердя. ММЛШ розраховували за формулою R. Dereveux et al.:
1,04 • [(TCMШПд + ТЗСМЛШд + КДР) • 3] – [КДР] • 3 – 13,6 [24].
Обчислення індексу товщини стінки міокарда ЛШ (ІТСМЛШ) є чутливішим параметром, що характеризує геометричний тип ремоделювання міокарда ЛШ (2Н/D):
ІТСМЛШ = (ТЗСМЛШд + ТСМШПд) / КДР.
Потім розраховували індекс маси міокарда лівого шлуночка за відношенням до росту пацієнтів:
ІММЛШ (г/м) = ММЛШ / Р,
де Р — ріст пацієнта у метрах.
Статистичну обробку даних проводили за допомогою програми Microsoft Exсel 2003. Аналіз даних передбачав оцінку нормальності розподілу змінних. Оскільки розподіл даних був відмінним від нормального, використовували непараметричний метод для оцінки пов’язаних вибірок (критерій знаків z). Зв’язок між показниками оцінювали за допомогою рангової кореляції Спірмена (rs). Статистичні показники представлені в таблицях таким чином: середнє арифметичне — похибка середнього арифметичного, n — об’єм групи, яку аналізують. Різницю між показниками вважали статистично значущою, якщо р < 0,05.
Результати дослідження
Дані клінічного обстеження хворих, показники центральної гемодинаміки, деякі імунологічні та метаболічні показники наведено в табл. 1.
/54/54.jpg)
Як видно з табл. 1, обстежені хворі були старшої вікової групи з наявністю ЦД в поєднанні з НАЖХП та АГ.
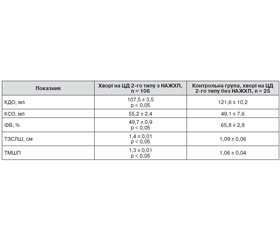
У хворих на ЦД в поєднанні з НАЖХП показники КДО, ФВ та ТЗСЛШ вірогідно відрізнялись від показників контрольної групи, що свідчить про вагомий внесок НАЖХП у структурно-функціональні зміни ЛШ (табл. 2).
Середній рівень ФНП-альфа в обстежених нами хворих становив 193,7 ± 7,5 пг/мл і більше ніж удвічі перевищував показники норми, рівень ІЛ-6 — 173,3 ± 11,0 пг/мл, що теж значно більше за норму.
Окремо нами були визначені показники вказаних цитокінів у жінок та чоловіків і проведено кореляційний аналіз між ФНП-альфа та ІЛ-6 у жінок і чоловіків та показниками центральної гемодинаміки (табл. 3).
Як видно з наведених у табл. 3 даних, у наших дослідженнях отримано негативний кореляційний зв’язок між ФНП-альфа та показниками КДО, КСО, КДР та КСР у чоловіків та ФНП-альфа і КДР та КСР у жінок, а також негативний кореляційний зв’язок між ІЛ-6 та КСР у чоловіків. Нами також було визначено показник відношення об’єму талії до об’єму стегон (ознаки наявності інсулінорезистентності), який у групі чоловіків становив 1,01 ± 0,07, а у жінок — 0,99 ± 0,02. Ці показники свідчать про наявність інсулінорезистентності в обстежених хворих.
Висновки
1. У хворих на цукровий діабет 2-го типу в поєднанні з неалкогольною жировою хворобою печінки відзначаються зміни структурно-функціональних показників лівого шлуночка, що проявляється зниженням кінцево-діастолічного об’єму і фракції викиду та збільшенням товщини задньої стінки лівого шлуночка та товщини міжшлуночкової перегородки.
2. В обстежених пацієнтів доведено значне збільшення цитокінів: фактора некрозу пухлини альфа та інтерлейкіну-6, що обумовлено наявністю інсулінорезистентності та дисліпідемією.
3. Визначено негативний корелятивний зв’язок між фактором некрозу пухлини альфа, інтерлейкіном-6 та показниками структурно-функціональних змін лівого шлуночка, що свідчить про значний вклад даних показників низькоінтенсивного запалення у процес ремоделювання міокарда.
1. Kozak B.M. International Diabetes Federation (IDF) highlights growing global impact of diabetes in 5th edition of the Diabetes Atlas [Text] / B.M. Kozak, M.Y. Tjota, K.L. Close // J. of Diabetes. — 2013. — Vol. 4. — P. 8–17.
2. Полторак В.В., Горшунська М.Ю., Красова Н.С. Адипонектин та цукровий діабет 2-го типу (патогенетичні аспекти як підґрунтя для оптимізації антидіабетичної фармакотерапії) [Текст] / В.В. Полторак // Международный эндокринологический журнал. — 2014. — № 5 (61). — С. 95–104.
3. American Diabetes Association (ADA). Diagnosis and Classification of Diabetes Mellitus [Text] / ADA // Diabetes Care. — 2012. — Vol. 35 (1). — P. S64–S71.
4. Gu K. Mortality in adults with and without diabetes in a national cohort of the U.S. population, 1971–1993 [Text] / K. Gu, C.C. Cowie, M.I. Harris // Diabetes Care. — 1998. — Vol. 21. — P. 1138–1145.
5. Bertoni A.G. Diabetes-related morbidity and mortality in a national sample of U.S. elders [Text] / A.G. Bertoni, J.S. Krop, G.F. Anderson, F.L. Brancati // Diabetes Care. — 2002. — Vol. 25. — P. 471–475.
6. Metabolite profiles and the risk of developing diabetes [Text] / T.J. Wang, M.G. Larson, R.S. Vasan [et al.] // Nat. Med. — 2011. — Vol. 17. — P. 448–453.
7. Однонуклеотидний поліморфізм гена адипонектину (+276Т) та експресія складових інсулінорезистентного стану у хворих на цукровий діабет 2 типу [Текст] / Ю.І. Караченцев, М.Ю. Горшунська, Н.О. Кравчун [та ін.] // Пробл. ендокрин. патології. — 2013. — № 2. — С. 7–17.
8. Ritchie S.A. The link between abdominal obesity, metabolic syndrome and cardiovascular disease [Text] / S.A. Ritchie, J.M. Connell // Nutr. Metabol. Cardiovasc. Dis. — 2007. — Vol. 17. — P. 319–326.
9. Musso G. Non-alcoholic fatty liver disease from pathogenesis to management: an update [Text] / G. Musso, R. Gambino, M. Cassader // Obesity Reviews. — 2010. — Vol. 11, № 6. — P. 430–445.
10. Pickup J.C. Inflammation and activated innate immunity in the pathogenesis of type 2 diabetes [Text] / J.C. Pickup // Diabetes Care. — 2004. — Vol. 27. — P. 813–823.
11. Wei S.G. Central SDF-1/CXCL12 expression and its cardiovascular and sympathetic effects: the role of angiotensin II, TNF-а, and MAP kinase signaling [Text] / S.G. Wei, Z.H. Zhang, Y. Yu, R.B. Felder // Am. J. Physiol. Heart Circ. Physiol. — 2014. — Vol. 307 (11). — P. 1643–1654.
12. Кравчун Н.О. Фактор некрозу пухлин та цукровий діабет [Текст] / Н.О. Кравчун // Пробл. ендокрин. патології. — 2005. — № 3. — С. 3–8.
13. Кравчун Н.О. Активність інтерлейкіну-6 у хворих на цукровий діабет 2 типу в залежності від варіанту перебігу захворювання [Текст] / Н.О. Кравчун // Пробл. ендокрин. патології. — 2005. — № 4. — С. 23–31.
14. Shoelson S.E. Inflammation and insulin resistance [Text] / S.E. Shoelson, J. Lee, A.B. Goldfine // J. Clin. Invest. — 2006. — Vol. 116. — P. 1793–1801.
15. A prospective study of soluble tumor necrosis factor alpha receptor II (sTNF-RII) and risk of coronary heart disease among women with type 2 diabetes [Text] / I. Shai, M.B. Schulze, J.E. Manson [et al.] // Diabet. Care. — 2005. — Vol. 28 (6). — P. 1376–1382.
16. Acute interleukin-6 administration does not impair muscle glucose uptake or whole-body glucose disposal in healthy humans [Text] / A. Sttensberg, P. Fischer, F. Christian [et al.] // J. Physiol. — 2003. — Vol. 548, № 2. — P. 631–638.
17. Чаяло П.П. Нарушение обмена липопротеидов [Текст] / П.П. Чаяло. — К.: Здоров’я, 1990. — 182 с.
18. Колб В.Г. Клиническая биохимия [Текст] / В.Г. Колб, В.С. Камышников. — Минск: Беларусь, 1976. — С. 171–174.
19. Методические указания к лабораторным работам по клинической биохимии [Текст] / Тр. Укр. ин-та усовершенствования врачей (каф. мед. биохимии). — Х., 1988. — С. 62–63.
20. Сравнительный анализ методов определения гликозилированного гемоглобина [Текст] / М.Н. Гришинин, В.А. Галенок, А.Г. Мазовецкий [и др.] // Лаб. дело. — 1988. — № 2. — С. 19–23.
21. Колб В.Г. Клиническая биохимия [Текст] / В.Г. Колб, В.С. Камышников. — Минск: Беларусь, 1976. — С. 117–120.
22. Определение фибриногена весовым методом [Текст] // Лабор. дело. — 1984. — № 5. — С. 273.
23. Определение фибрина спектрофотометрическим методом [Текст] / В.А. Белицер, И.В. Варецкая, Ю.В. Бутылин [и др.] // Лабораторное дело. — 1983. — № 4. — С. 38.
24. Зайцева В.И. Синдром инсулинорезистентности и его значение в кардиологической практике [Текст] // В.И. Зайцева / Укр. кардіол. журн. — 2000. — № 5–6. — С. 114–117.
25. Полозова Л.Г. Факторы, определяющие прогноз при инфаркте миокарда у больных с инсулинонезависимым сахарным диабетом [Текст] // Л.Г. Полозова / Укр. кардіол. журн. — 2000. — № 3. — С. 24–26.

/55/55.jpg)