Одна зі значних ініціатив Всесвітньої організації охорони здоров’я (ВООЗ) і Дитячого фонду Організації Об’єднаних Націй спрямована на глобальне просування, захист і підтримку грудного вигодовування [1]. Це пов’язано з тим, що хоча і медичні працівники, і самі матері знають, що грудне молоко є оптимальним для годування немовлят, показники грудного вигодовування значно нижчі від рекомендованих ВООЗ, особливо в урбанізованих, економічно розвинених країнах. Американська колегія акушерів і гінекологів (ACOG), Американська академія педіатрії (AAP) та Американська академія сімейних лікарів (AAFP) рекомендують перші 6 місяців виключно грудного вигодовування для всіх немовлят [2, 3].
ВООЗ наполегливо рекомендує виключно грудне вигодовування дитини до 6-місячного віку, потім введення прикорму після 6 місяців і продовження грудного вигодовування до 2-річного віку дитини або стільки часу, скільки це потрібно обом (матері й дитині) [4], такі рекомендації обумовлені численними багатоцентровими клінічними спостереженнями й клінічними дослідженнями про користь грудного вигодовування як для дитини, так і для матері [5–7].
Одні з найбільш важливих доказів користі грудного вигодовування немовляти не менше за 6 місяців отримані в масштабному кластерному рандомізованому дослідженні PROBIT, у якому спостерігали за станом здоров’я матері й дитини в перші 12 місяців після народження, а для понад 80 % пар «мати і дитина» спостереження вели 11,5 року. Дослідження PROBIT показало, що грудне вигодовування, заохочення до нього матері, стимулювання лактації натуропатичними методами, впровадження в клініки проєкту «Лікарня доброзичливого ставлення до дитини» (BFHI) збільшує тривалість грудного вигодовування (до 2 років), період виключно грудного вигодовування (до 6 місяців) і знижує ризик розвитку в дитини шлунково-кишкових інфекцій, атопічної екземи в дитинстві, а також позитивно корелює з більш високими показниками інтелекту в дитини у віці 6,5 року [8].
У дослідженні А. Fiocchi (2015) [9] доведено, що в дітей, які знаходяться не менше ніж 6 місяців на грудному вигодовуванні, формується адекватна мікробіота шлунково-кишкового тракту, що вірогідно порівняно з плацебо знижує ризик розвитку в перші три роки життя харчової алергії (р < 0,05), атопічного дерматиту (р < 0,05), бронхіальної астми (р < 0,05), алергічного риніту (р < 0,05) і алергічних захворювань сумарно (р < 0,05), ефект посилюється, якщо матері, які годують груддю, отримували пробіотик.
Більшість дослідників резюмують, що для дітей грудного віку відсутність грудного вигодовування або більш раннє його припинення пов’язані зі збільшенням частоти інфекційних захворювань, включно з отитом середнього вуха, гастроентеритом і пневмонією, а також підвищеним ризиком дитячого ожиріння, діабету 1-го і 2-го типу, лейкемії і синдрому раптової дитячої смерті [10, 11].
Ретроспективні епідеміологічні дослідження показують, що діти, яких годують молочною сумішшю в дитинстві, частіше страждають від ожиріння або хворіють на діабет 2-го типу. У метааналізах доведено, що використання дитячої суміші для годування в дитинстві підвищувало ризик ожиріння від 1,1 (95% довірчий інтервал (ДІ) 1,0–1,1) до 1,3 (95% ДІ 1,2–1,5) раза порівняно з дітьми, які будь-коли перебували на грудному вигодовуванні. Використання суміші в дитинстві також пов’язане з 1,6-кратним ризиком (95% ДІ 1,2–2,3) розвитку діабету 2-го типу порівняно з грудним вигодовуванням [12, 13].
Якщо грудне вигодовування має першорядне значення для доношених здорових новонароджених, воно ще більш важливе для новонароджених з високим ризиком, наприклад для немовлят, які народилися з низькою і/або дуже низькою масою тіла, а також для новонароджених, які з різних причин перебували в перші дні життя в відділеннях інтенсивної терапії. Ризики, пов’язані з відсутністю грудного вигодовування таких новонароджених, добре відомі й включають вищі показники некротичного ентероколіту, інфекційних (включно з вірусними) захворювань з тяжким перебігом. Якщо такі немовлята не отримують зцідженого грудного молока, то вони мають вірогідно більш низькі результати тестів на розвиток нервової системи, більш високий показник смертності. З іншого боку, необхідно відзначити, що в клініках усього світу показники грудного вигодовування нижчі саме в умовах відділення інтенсивної терапії [14–16]. Відсутність грудного вигодовування негативно позначається і на здоров’ї матері.
Безпосередньо після пологів молочні залози починають виділяти молозиво — рідину жовтуватого кольору, що містить клітини альвеол, велику кількість білків (глобулін), невелику кількість жиру, антитіла (зокрема, імуноглобулін A) та інші речовини. Надалі безперервна секреція молока контролюється нейрогуморальним шляхом (надлишок естрогенів пригнічує лактогенез), у проміжках між годуванням груддю пролактин стимулює утворення й резервування молока для наступного годування. Виділення молока із соска молочної залози являє собою рефлекторну реакцію (let-down reflex; milk-ejection reflex) взаємодії матері й дитини. Коли немовля смокче груди, відбувається стимуляція сенсорних рецепторів соска, далі інформація про це надходить через спинний мозок матері до її гіпоталамуса, у якому нейросекреторні клітини виділяють окситоцин, останній потрапляє в кровоносне русло матері через задню частку гіпофіза. Окситоцин викликає скорочення міоепітеліальних клітин, що оточують молочні альвеоли. Молоко, що міститься в порожнині молочних альвеол, через молочні протоки й синуси виштовхується із сосків грудної залози матері.
Стадії лактогенезу в модифікації J. Riordan [17] подані в табл. 1.
Загальновідомо, що лактація пригнічує овуляцію, приводячи до лактаційної аменореї. Крім того, лактогенез приводить до термінального диференціювання тканини молочної залози з потенційним довгостроковим впливом на злоякісну трансформацію. Ці ефекти можуть опосередковувати зв’язок між грудним вигодовуванням і раком молочної залози і яєчників.
Лактогенез — природний фізіологічний процес, до якого організм жінки готується вже із середини вагітності, тому повна відмова від грудного вигодовування або вкрай короткий період годування (1–2 місяці) можуть мати негативні наслідки для організму жінки.
Деякі дослідження припускають, що грудне вигодовування знижує ризик розвитку раку молочної залози [18]. Метааналіз 47 досліджень показав, що тривале грудне вигодовування (не менше від 12 місяців) асоціюється зі зниженням ризику розвитку інвазивного раку молочної залози на 4,3 % (95% ДІ 2,9–5,8) [19].
У дослідженні A.M. Stuebe зі співавт. (2009) встановлено, що в групі жінок, які ніколи не годували груддю, у пременопаузі в 2,4 раза більше діагностувався рак молочної залози (95% ДІ 1,3–4,5) порівняно з тими, хто будь-коли годував груддю [20]. Також є дані, що для матерів відмова від грудного вигодовування пов’язана з підвищенням частоти виникнення раку яєчників, збереженням збільшеної ваги, набраної під час вагітності, розвитком діабету 2-го типу й метаболічного синдрому [4].
Отже, спираючись на рекомендації ВООЗ, профільних асоціацій, результати клінічних досліджень, можна стверджувати, що грудне вигодовування немовляти від 6 місяців до 2 років має доведений позитивний вплив на здоров’я і розвиток дитини і на здоров’я матері.
Основною причиною об’єктивних відмов від грудного вигодовування, за даними В.К. Юр’єва і співавт. (2019) [21], була відсутність у матері молока, питома вага якої була максимальною в 3 місяці і поступово знижувалася до 12 місяців (від 56,4 до 36,7 % відповідно). Найчастіше жінки припиняли грудне вигодовування в 3 і 6 місяців життя дитини (21,8 і 25,3 % відповідно). Основними суб’єктивними причинами припинення годування дитини грудним молоком на першому році були необхідність виходу на навчання або роботу (11,6 %) і небажання жінки продовжувати грудне вигодовування (9,1 %).
Значна питома вага відмов від грудного вигодовування, яким можна було запобігти, є показником незадовільної роботи служби охорони материнства й дитинства з підтримки й популяризації грудного вигодовування, відсутність об’єктивної інформації в гінекологів, педіатрів, сімейних лікарів про сучасні натуропатичні препарати, здатні оптимізувати лактогенез.
Ефективним і безпечним вирішенням проблем грудного вигодовування може бути застосування жінкою, яка годує груддю, натуропатичного засобу Мамолакт.
Мамолакт містить екстракти Pueraria tuberosa, Trigonella foenum-graecum, Asparagus racemosa, Leptadenia reticulata, Withania somnifera, Allium sativum і вітальний мікроелемент цинк. Такий склад натуропатичного засобу не тільки стимулює лактогенез, насичує молоко корисними речовинами, що благотворно впливає на імунну систему матері й дитини, але й допомагає відновленню гормонального балансу в організмі жінки і чинить легку заспокійливу дію. Доцільно більш детально розглянути компоненти натуропатичного засобу Мамолакт.
Багаторічна рослина Pueraria tuberosa (пуаерія горбиста) широко відома як відариканда, поширена по всій Південно-Східній Азії. У бульбах Pueraria tuberosa виявлені численні біологічно активні речовини (БАР), в основному ізофлавоноїди, такі як пуерарин, геністеїн, даїдзеїн, туберозин тощо. Дослідження in vivo та in vitro підтвердили наявність імуностимулюючої, протизапальної дії. Здатність позитивно впливати на жіночу репродуктивну сферу зумовила застосування екстракту цієї рослини при порушеннях фертильності, менопаузальному синдромі [22].
Однією з основних діючих речовин екстракту Pueraria tuberosa є ізофлавоноїд пуерарин (7-hydroxy-3-(4-hydroxyphenyl)-8-[(3R,4R,5S,6R)-3,4,5-trihydroxy-6- (hydroxymethyl)oxan-2-yl]chromen-4-one), виділений із рослини в кінці 1950-х років. З того часу його фармакологічні властивості були ретельно досліджені. Лікувально-профілактичні ефекти пуерарину пов’язані з його широким спектром фармакологічних властивостей, таких як вазодилатація, кардіозахист, нейрозахист, антиоксидантна, протипухлинна, протизапальна, помірна аналгетична дія. Також є дані досліджень про те, що пуерарин сприяє формуванню кісткової тканини й поліпшує метаболізм (знижує інсулінорезистентність) [23].
Не менш значущою БАР екстракту Pueraria tuberosa на сьогодні вважається флавоноїдоподібна сполука ізоорієнтин ((1S)-1,5-anhydro-1-[2-(3,4-dihydroxyphenyl)-5,7-dihydroxy-4-oxo-4H-chromen-6-yl]-D-glucitol), для якої характерна виражена актиоксидантна дія і помірна протизапальна активність за рахунок селективного інгібування циклооксигенази-2, що було підтверджено на різних моделях K. Anilkumar і співавт. (2017) [24]. Автори дослідження підкреслюють фізіологічно лояльний механізм антиоксидантної дії, що реалізується за рахунок активації ферментативної (каталаза) і неферментативної (відновлений глутатіон) ланки ендогенної антиоксидантної системи захисту організму.
Важливим фактором для натуропатичного засобу, призначеного для застосування жінками в період годування груддю, є антигіпоксична активність компонентів. Гіпоксія, у сучасному розумінні, — це процес порушення оптимальної енергопродукції. Дефіцит енергії призводить до якісно однотипних метаболічних і структурних зрушень у різних органах і тканинах, особливо чутливих до гіпоксії (мозок, серце, нирки, печінка). На думку низки авторів, навіть вагітність, що «перебігає ідеально», пологи, а також період після пологів, годування груддю супроводжуються підвищеними потребами клітини в енергопродукції і різними за ступенем вираженості проявами гіпоксії [25].
За даними R. Shukla (2017) [26], БАР екстракту Pueraria tuberosa проявляють високу антигіпоксичну активність, навіть в умовах украй тяжкої діабетичної нефропатії.
Екстракт Trigonella foenum-graecum отримують з давно відомої в медицині однорічної рослини гуньби сінної (сімейство бобові). Насіння гуньби сінної містить слиз, тригонелін, 4-гідроксиізолейцин, сотолон, діосгенін, лютеолін, фенольні кислоти й протодіосцин.
Екстракт Trigonella foenum-graecum (або насіння гуньби сінної) давно використовується в низці географічних регіонів у всьому світі як лактогенний засіб для збільшення кількості та якості молока і включений у численні патентовані фітосуміші, які просуваються для збільшення кількості молока [27].
У дослідженні S. Kavurt [28], у якому взяли участь 80 жінок (18–35 років), установлено, що застосування гуньби сінної посилює лактацію й антиоксидантний статус грудного молока.
В опублікованому T.M. Khan (2017) [29] систематичному огляді на підставі проведеного мережевого метааналізу клінічних досліджень було виявлено п’ять досліджень із 122 учасниками, жінками, які отримували екстракт гуньби сінної в період годування груддю. Результати досліджень переконливо довели, що застосування екстракту гуньби сінної значно збільшує кількість продукованого грудного молока (11,11; ДІ 95% 6,77–15,46) порівняно з жінками, які годують груддю, із групи плацебо-контролю.
Наявна в літературі інформація про користь для здоров’я і терапевтичні ефекти Trigonella пояснює її відомі лікувальні властивості й додає нові показання до застосування. Крім відомих лікувальних властивостей, таких як вітрогонний, шлунковий, протидіабетичний і галактогенний (індуктор лактації) ефекти, більш нові дослідження виявили гіпохолестеринемічний, антиліпідемічний, антиоксидантний, гепатопротекторний, протизапальний, лікувальні ефекти гуньби сінної. Екстракт гуньби сінної знижує рівень холестерину й глюкози, відновлює концентрацію глікогену в печінці, а отже, активує жировий обмін і допомагає в зниженні надмірної ваги. Біологічно активні речовини й мікроелементи, які містить екстракт насіння гуньби сінної, мають нейропротекторну дію, поліпшують пам’ять і роботу мозку [30].
Уведений до складу Мамолакту екстракт Asparagus racemosa отримують з рослини спаржа гроноподібна, що росте в передгірних районах Індії, у Гімалаях, ботанічно описаної ще в 1799 р. Екстракт містить у малих дозах збалансований склад БАР: стероїдні сапоніни, шатаварозид A, шатаварозид B, філіаспарозид C, шатаварини, імунозид і шидигерасапонін D5 (або аспаранін A), а також ізофлавон-8-метокси-5,6,4’-тригідроксиізофлавон-7-O-β-D-глюкопіранозид [31].
У дослідженні A.K. Рandey і співавт. (2018) [32] наведені дані, що шатаварини екстракту Asparagus racemosa поліпшують показники жіночого репродуктивного здоров’я на тлі різних ускладнень, що включають гормональний дисбаланс, синдром полікістозних яєчників, ріст і розвиток фолікулів, якість ооцитів і безплідність, за рахунок зниження рівня оксидативного стресу й підвищення рівня ендогенних антиоксидантів в організмі.
Підтвердження передбачуваного антиоксидантного механізму дії, що переважно відповідає за терапевтичні ефекти екстракту спаржі, наведені в численних роботах, зокрема в дослідженні С. Onlom (2017) [33]. Виділені з Asparagus racemosus стероїдні сапоніни шатаварин I і шатаварин IV мають виражену антиоксидантну дію і здатні знижувати активність процесів перекисного окиснення ліпідів в організмі в умовах оксидативного стресу.
Висока антиоксидантна активність БАР екстракту Asparagus racemosa підтверджена in vitro [34] з використанням різних методів, таких як антирадикальна активність щодо видалення (нейтралізації) гідроксильних радикалів і активність щодо поглинання оксиду азоту. Встановлено, що екстракт спаржі гроноподібної в дозі 500 мкг/мл in vitro проявляє максимальну антирадикальну активність.
БАР спаржі гроноподібної, як доведено в дослідженні P.L. Srivastava (2018) [35], усувають гормональний дисбаланс у жінок. Дані біологічно активні речовини, у першу чергу за рахунок відновлення балансу фолікулостимулюючого і лютеїнізуючого гормонів у гіпоталамо-гіпофізарній системі, впливають на синтез прогестерону в яєчниках і втручаються в процес біотрансформації естрогену, сприяючи стимуляції перетворення естрадіолу в малоактивний естрон.
Екстракт Leptadenia reticulata, отриманий із лептаденії сітчастої (Asclepiadaceae), налічує тисячолітню історію застосування в аюрведичній медицині під назвою «дживанті» й успішно застосовується для збільшення лактації. Офіційна медицина звернула увагу на цю лікарську рослинну сировину порівняно недавно, коли починаючи з 60-х років минулого століття на медичному ресурсі PubMed стали з’являтися публікації про ці компоненти [36].
В аюрведі є наука під назвою «расаяна», що займається поліпшенням загального стану здоров’я, бадьорості й життєздатності. Серед різних трав, які використовуються в расаяні, Leptadenia reticulata (Jivanti) посідає унікальне місце, що зумовлене її відновлювальними, омолоджувальними властивостями для жіночого організму й значним лактогенним ефектом [37].
Терапевтичний потенціал цієї рослини зумовлений наявністю різних біологічно активних сполук із класу флавоноїдів і тритерпенових сапонінів, таких як α-амірин, β-амірин, ферулова кислота, лютеолін, діосметин, рутин, β-ситостерин, стигмастерол, хентриконтанол, тритерпеновий спирт, симіаренол, апігенін, ретикулін, лупеол, денікулатин і лептакулатин [38].
На сьогодні у фармакологічних дослідженнях доведена здатність екстракту Leptadenia reticulata стимулювати вироблення молока в жінок, які годують груддю, і поліпшувати його якість, підтверджені сечогінна дія, гепатопротекторна й кардіопротекторна активність, омолоджувальний ефект, а також м’яка анксіолітична й антидепресивна дія [39].
Уперше лактогенну дію екстракту було згадано в 1947 році в клінічному дослідженні N.V. Patel [40], який уперше повідомив про корисність Leptadenia reticulata в аспекті репродуктивного здоров’я жінки, запобігання звичним викидням, а також підтвердив лактогенну властивість цієї рослини. Пізніше з’явилися дані, що підтверджують виражену лактогенну дію таблеток лептадену на основі екстракту L.reticulata [41].
Наступні клінічні дослідження показали, що в більшості випадків лептаден стимулював лактацію протягом 12 годин після прийому першої дози екстракту [42].
Механізм лактогенної дії L.reticulata реалізується за рахунок того, що стигмастерин і інші тритерпени стимулюють активність альвеолярної тканини грудної залози, а якість грудного молока поліпшується за рахунок збільшення в ньому відсоткового вмісту жиру [43].
Наступний компонент Мамолакту — це екстракт Withania somnifera, отриманий із рослини ашваганда (сімейство Solanacea), що росте в Індії, Пакистані, Південно-Західній Азії і Європі і широко використовується у світі аюрведичної медицини завдяки своїм численним цілющим властивостям.
Біохімічні складові Withania somnifera, такі як вітанолід A, вітанолід D, вітаферин A і вітаніаміди, відіграють важливу роль у фармакологічних властивостях даного екстракту. Такі білки, як глікопротеїн вітанії сомніфера і лектиноподібний білок вітанії, мають потужні терапевтичні властивості, такі як нейропротективна, м’яка седативна, а також антигепатотоксична, антигіпоксична й антиоксидантна дія [44].
В одному з останніх оглядів N.J. Dar (2015) [45] узагальнені дані щодо фармакогностичного й фармакологічного профілю W.somnifera, яку також називають індійським женьшенем, — однієї з важливих лікарських рослин Індійського субконтиненту. У сучасних доклінічних дослідженнях екстракт ашваганди продемонстрував антистресові, нейропротекторні, кардіозахисні й антидіабетичні властивості. Крім того, він продемонстрував здатність зменшувати кількість активних форм кисню, модулювати функцію мітохондрій, регулювати апоптоз, зменшувати запалення й поліпшувати функцію ендотелію. Дані про позитивний вплив екстракту Withania somnifera на репродуктивну сферу наведені в роботі R. Nasimi Doost Azgomi (2018) [46], автори пояснюють його позитивним впливом екстракту на баланс фолікулостимулюючого й лютеїнізуючого гормонів.
У дослідженні Т. Kuboyama (2014) [47] доведено, що екстракт ашваганди в системі in vitro стимулює зростання нейритів. Вітанолід A, вітанозид IV і вітанозид VI ідентифіковані як нейроактивні компоненти екстракту, що індукували зростання нейритів в ізольованих клітинах нейробластоми людини SH-SY5Y і нейронах кори головного мозку щура. В експериментальній моделі атрофії аксонів in vitro, що була відтворена з використанням активного часткового фрагмента аксона Aβ25-35, вітанолід А, вітанозид IV і вітанозид VI, якими індивідуально обробляли атрофовані аксони, продемонструвати здатність значно індукувати ріст аксонів. Подібні нейропротективні властивості БАР ашваганди підтверджені на моделі синаптичної дегенерації in vitro. Пероральне введення вітаноліду A, вітанозиду IV або вітанозиду VI протягом 12 днів збільшувало щільність аксонів і синапсів у тім’яній корі головного мозку й усувало дефіцит просторової пам’яті.
У пілотному дослідженні D. Сhoudhary (2017) [48], проведеному на 50 дорослих учасниках з додатковою групою плацебо-контролю, провели оцінку ефективності й безпеки екстракту ашваганди (300 мг два рази на день) або плацебо протягом восьми тижнів. Вивчали показники пам’яті й когнітивних функцій. Після восьми тижнів дослідження група лікування ашвагандою продемонструвала значне поліпшення порівняно з групою плацебо як щодо негайної, так і щодо загальної пам’яті, про що свідчать бали субтеста за шкалою пам’яті Векслера III для логічної пам’яті I (p = 0,007), вербальних парних партнерів I (p = 0,042), обличчя I (p = 0,020), сімейних образів I (p = 0,006), логічної пам’яті II (p = 0,006), вербальних парних асоціацій II (p = 0,031), обличчя II (p = 0,014) і сімейних фотографій II (p = 0,006). Група, яка отримувала екстракт ашваганди, також продемонструвала значно більше поліпшення керуючих функцій, стійкої уваги й швидкості обробки інформації, про що свідчать оцінки за завданням Еріксена Фланкера (p = 0,002), тесту сортування карток Вісконсіна (p = 0,014), частини тесту Trail-Making A (p = 0,006) і тесту Mackworth Clock (p = 0,009). Встановлено, що екстракт ашваганди може бути ефективним засобом поліпшення як негайної, так і загальної пам’яті, а також поліпшення керуючих функцій, уваги й швидкості обробки інформації.
Важливим позитивним ефектом екстракту Withania somnifera, особливо для жінок, які виховують дитину перших років життя, є здатність даного екстракту збільшувати м’язову силу, знижувати м’язове ушкодження при високих фізичних навантаженнях (показник — стабілізація сироваткового ферменту креатинкінази), що встановлено в дослідженні S. Wankhede (2015) [49].
Екстракт Allium sativum (часник, Allium sativum L. fam. Alliaceae) — один із найбільш досліджених і таких, що користуються найбільшим попитом, рослинних продуктів на світовому фармацевтичному ринку. Сполуки, що містяться в часнику, синергічно впливають одна на одну, активні інгредієнти часнику включають ферменти (наприклад, аліїназу), сірковмісні сполуки, такі як аліїн, або сполуки, одержані ферментативним шляхом з аліїну (наприклад, аліцин). Концентрація аліцину (основного активного інгредієнта) і джерело характерного запаху часнику залежать від способу обробки. Аліцин нестабільний і досить швидко перетворюється в інші хімічні речовини. Документально підтверджено, що продукти, отримані навіть без аліцину, дають значний біологічний ефект щодо поліпшення імунної системи, лікування серцево-судинних захворювань, раку, печінки тощо. Багато доступних публікацій вказують на можливі антибактеріальні, гіпотензивні й антитромботичні властивості часнику [50].
З високим ступенем вірогідності в різних публікаціях доведена антимікробна й антиоксидантна активність екстракту Allium sativum, остання реалізується за рахунок полісахаридів, які мають β-глікозидний зв’язок і мають здатність вловлювати супероксид-аніони й гідроксильні радикали [51, 52].
Цинк, введений до складу натуропатичного засобу Мамолакт, є одним із найважливіших вітальних (життєво необхідних) мікроелементів. Дефіцит цинку, що може реєструватися в дитини з перших днів життя, становить серйозну проблему для охорони здоров’я усього світу. Тяжкий дефіцит цинку призводить до розвитку дерматитів, втрати ваги, діареї (може стати причиною смерті новонародженого), збільшення ризику зараження інфекційними захворюваннями [53].
У ранньому неонатальному періоді життя адекватним джерелом цинку є грудне молоко. Дефіцит цинку в грудному молоці — потенційно смертельне явище для дитини. Дефіцит цинку може порушити роботу імунної системи й підвищити схильність до розвитку інфекційної діареї, пневмонії та інших смертельно небезпечних для новонародженого захворювань. Дефіцит цинку як мінімум у двох поколінь може викликати епігенетичні ефекти, які змінюють експресію генів, що може бути однією з причин багатьох хронічних патологій у дорослому віці [54].
На сьогодні існує значно поширена глобальна недостатність поживних мікроелементів (НПМ), яка найбільше поширена й найбільш небезпечна для вагітних жінок і їхніх дітей віком до 5 років. НПМ є частою причиною порушення росту дитини, інтелектуальних порушень, перинатальних ускладнень і підвищеного ризику захворюваності й смерті. Дефіцит цинку є основною причиною летальної діареї новонароджених [55].
Особливо важливо не допустити цинк-дефіцитних станів у недоношених, ослаблених або немовлят, які народилися зі зниженою масою тіла. Сучасні уявлення про потреби в цинку недоношених дітей засновані на дослідженнях, проведених понад 25 років тому. З огляду на те, що в даний час частіше виживають більш недоношені діти, важливо звернути увагу на останні дані про частоту дефіциту цинку в немовлят з дуже низькою масою тіла (ДНМТ) при народженні. У дослідження К. Wulf (2013) [56] ретроспективно були включені 226 дітей з ДНМТ, які народилися в період із липня 2005 р. по грудень 2009 р. Середній гестаційний вік (ГВ) становив 28,7 тижня (діапазон від 23,0 до 38,0), а середня вага при народженні — 1120 г (діапазон 354–1495 г). Усі немовлята отримували добавки цинку відповідно до рекомендацій ESPGHAN. 26 (11,5 %) пацієнтів мали клінічні ознаки дефіциту цинку, з яких 15 мали сироваткові концентрації цинку < 50 мкг/дл, 9 — від 50 до 70 мкг/дл і 2 — > 70 мкг/дл. У немовлят з дерматитом концентрації були значно нижче (у середньому 26,7 мкг/дл, діапазон 19–31 мкг/дл) порівняно з немовлятами з діареєю або ізольованим периферичним набряком (35,3 і 51,8 мкг/дл відповідно). Найсильнішими незалежними факторами ризику були низький ГВ, невелика вага для ГВ і болі в дитини через резекцію кишечника внаслідок некротичного ентероколіту. Частота концентрацій цинку < 50 мкг/дл була розрахована як 6,6 % у немовлят із ДНМТ. Незважаючи на те, що дотримувалися поточних рекомендацій щодо додавання цинку, частота дефіциту цинку виявилася несподівано високою в немовлят зі зниженою масою тіла і ДНМТ. Незважаючи на ретроспективний характер цього одноцентрового дослідження, отримані дані переконливо свідчать про необхідність перегляду рекомендацій щодо додавання цинку для немовлят.
Як заявлено в одному з останніх оглядів, присвячених цинк-дефіцитним патологіям, S. Choi (2018) [57], зв’язок між дефіцитом цинку й розвитком серцево-судинних захворювань підтверджений численними дослідженнями. Вживання цинку у вигляді дієтичних добавок може істотно знизити ризик атеросклерозу й захистити від інфаркту міокарда та ішемії/реперфузійного ушкодження.
Слід зазначити, що всі рослинні екстракти (Pueraria tuberosa, Trigonella foenum-graecum, Asparagus racemosa, Leptadenia reticulata, Withania somnifera, Allium sativum), які входять до складу натуропатичного засобу Мамолакт, дозволені для застосування жінкам у період годування груддю (ресурс e-lactation.com), що є підтвердженням високого профілю безпеки.
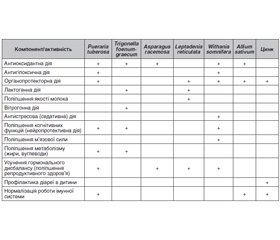
У табл. 2 поданий узагальнений профіль фармакологічної активності натуропатичного засобу Мамолакт.
Отже, проведений аналіз доступних фармакологічних досліджень (доклінічних, клінічних) кожного з компонентів (екстракти Pueraria tuberosa, Trigonella foenum-graecum, Asparagus racemosa, Leptadenia reticulata, Withania somnifera, Allium sativum, вітальний мікроелемент цинк) натуропатичного засобу Мамолакт дозволяє зробити такі висновки:
— Мамолакт стимулює лактацію і поліпшує якість молока (підвищує відсоткове співвідношення жирів, насичує молоко життєво необхідним для дитини вітальним елементом цинком);
— компоненти натуропатичного засобу надають комплексну органопротекторну й нейропротекторну дію з м’яким седативним ефектом;
— застосування даного засобу може сприяти поліпшенню роботи імунної системи в матері й дитини;
— компоненти, що входять до складу Мамолакту, поліпшують репродуктивне здоров’я матері, нормалізують гормональний баланс;
— антиоксидантна й антигіпоксична активність компонентів знижує оксидативний стрес і гіпоксичні прояви різного генезу, поліпшує роботу органів і систем у матері й дитини;
— безпека компонентів при застосуванні жінками, що годують груддю, підтверджена даними, що знаходяться на ресурсі e-lactation.com.
Конфлікт інтересів. Не заявлений.
Отримано/Received 01.02.2021
Рецензовано/Revised 11.02.2021
Прийнято до друку/Accepted 20.02.2021

/47.jpg)
/51.jpg)